微流场技术在酶催化扁桃酸酯水解反应中的应用毕业论文
2020-04-15 22:01:32
摘 要
ABSTRACT 2
前言 3
第一章 绪论 4
1.1、扁桃酸 4
1.2,酶 4
1.2.2酶催化在手性合物成中的应用 4
1.2.3 酶催化的不对称水解反应 5
1.2.4脂肪酶 5
1.3.微流场 6
1.3.1微流场的优点 6
第二章 实验思路与实验准备 6
2.1实验思路来源 6
2.2实验仪器及试剂 7
2.2.1实验仪器 7
2.2.2实验试剂 7
第三章 试验线路及条件筛选 8
3.1试验线路 8
3.1.1反应路线 8
3.2优化反应条件 10
3.2.1溶剂的摸索 10
3.2.2酶的摸索 10
3.2.3底物浓度的筛选 11
3.2.4温度的选择 11
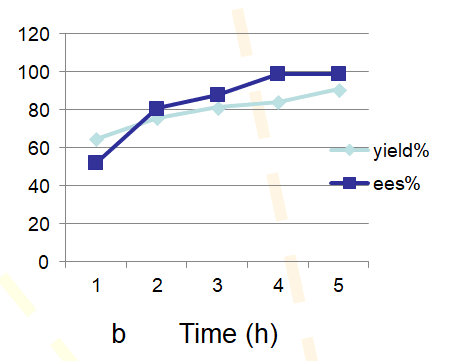
3.2.5反应时间的选择 12
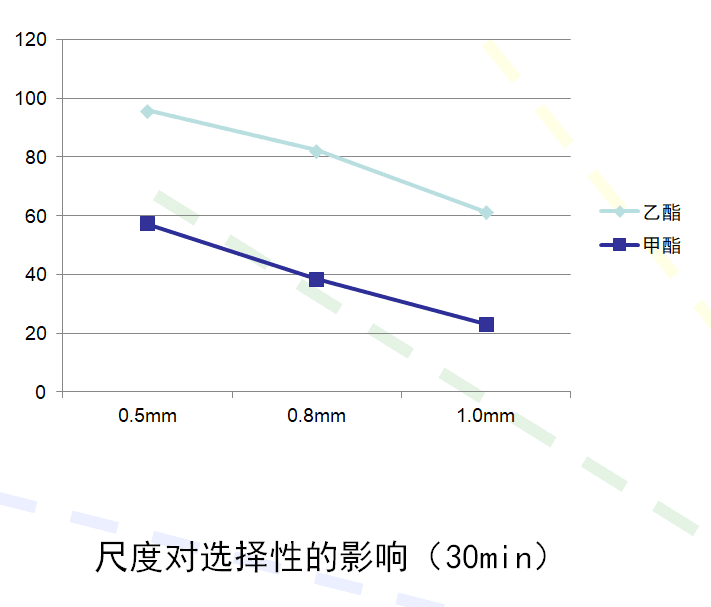
3.2.6管径的筛选 12
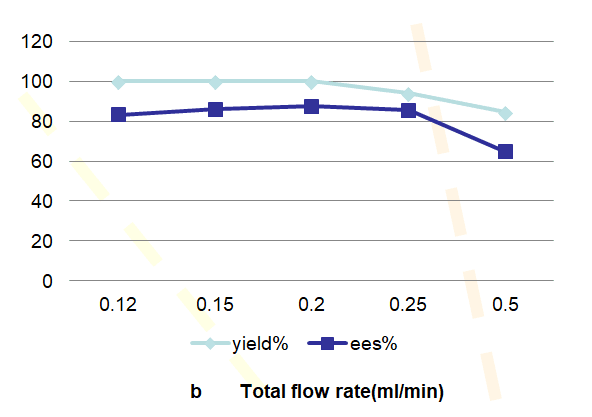
3.2.7流速比的选择 13
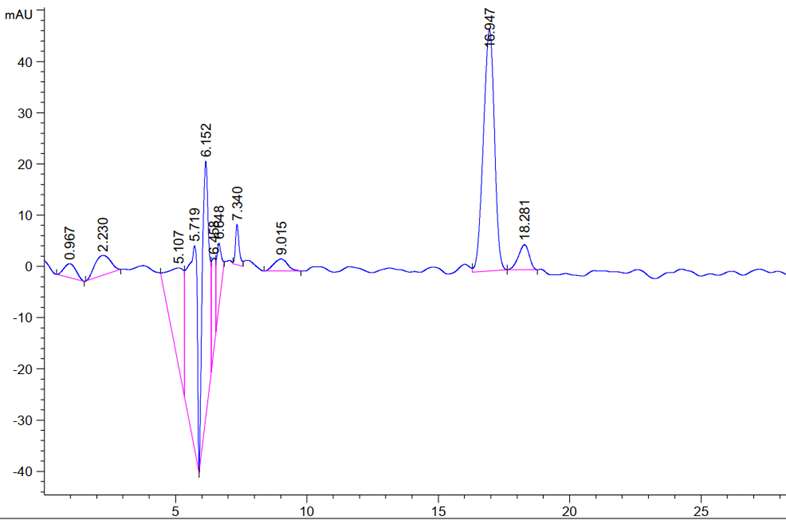
3.2.8保留时间 14
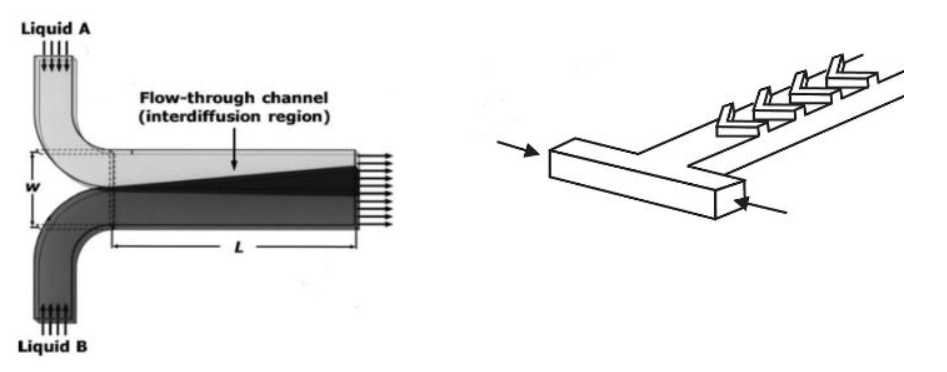
3.2.9混合器类型的选择 14
3.3总结 15
3.3.1最优反应条件 15
3.3.2后处理步骤 15
第四章 底物延伸与机理分析 16
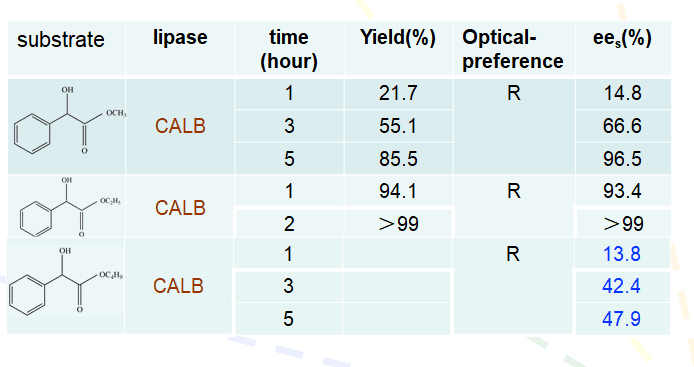
4.1扁桃酸酯的扩展 16
4.2机理讨论 17
第五章 总结 18
参考文献 19
附 录 21
致谢 24
微流场技术在酶催化扁桃酸酯水解反应中的应用
摘要
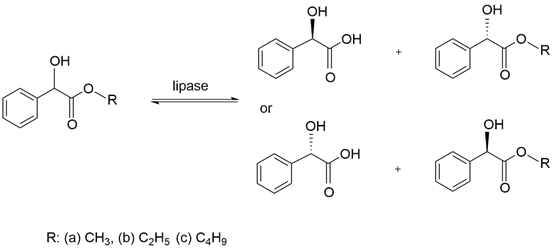
扁桃酸具有R、S两种构型,其中R-(-)-扁桃酸是一种关键的手性中间体,在多种药物的合成中均有广泛应用,也可作为手性试剂,拆分其它手性化合物。因此,手性扁桃酸成为热点的精细化工中间体。传统方法合成扁桃酸有产率低,选择性差,环境破坏大等缺点。而利用生物方法制备光学纯的扁桃酸具有立体、区域和化学选择性较高,并有着能完成一些难以用化学方法进行的反应等优点。本实验采用假丝酵母脂肪酶在微流场中水解扁桃酸酯的方法制备扁桃酸,该反应具有反应条件温和易控制,环境友好等优点。
关键词:扁桃酸 手性 假丝酵母酶 水解 微流场技术
Application of Microfluidic Field Technology in Enzymatic Catalyzed Hydrolysis of Mandelic Acid
ABSTRACT
Mandelic acid has two configurations of R and S, among which R-(-)-mandelic acid is an important chiral intermediate, which is widely used in the synthesis of various drugs, and can also be used as a chiral reagent. Divided into other chiral compounds. Therefore, chiral mandelic acid has become a hot chemical intermediate. The traditional method for synthesizing mandelic acid has the disadvantages of low yield, poor selectivity and large environmental damage. The use of biological methods for the preparation of optically pure mandelic acid has the advantages of high stereo, regional and chemical selectivity, and can accomplish some reactions that are difficult to carry out by chemical methods. In this experiment, mandelic acid was prepared by hydrolyzing mandelic acid ester in a microfluidic field by Candida lipase. The reaction has the advantages of mild and easy control of reaction conditions and environmental friendliness.
Key words: mandelic acid;chirality; CALB; hydrolysis;microfluidic field technology
前言
扁桃酸一种是极其重要的手性药物中间体,普遍运用于医疗药物生产、农业化学品合成、化工原料等领域,目前市场需求越以每年10%的速度快速增长,其中R-(-)-扁桃酸及其衍生物是合成抗抑郁药物、血管扩张剂等的重要药物中间体,同时兼具良好的生物分解性,是当下最受关注的光学拆分剂之一。
当下光学纯扁桃酸的生产方法主要有:物理化学方法主要为毛细管电泳法和色谱分离法,但由于手性添加剂价格高昂,难以大规模的工业化生产;化学拆分法一般利用生物碱、手性胺等与扁桃酸形成非对映体盐结晶从而进行拆分,缺点是产品收率偏低,反应步骤过多,环境污染,反应条件难以控制等。
生物法主要通过水解酶,对扁桃酸外消旋体酯化得到的扁桃酸酯进行水解,获取单一对应性扁桃酸。然而目前生物法受限于酶活力低,反应拆分效果不够理想,暂时达不到工业生产水平。我们在此基础上引入了微流场技术进行优化。
传统的化学反应过程是间歇性的,反应和纯化效率太低,环境污染物排放过多,工艺流程路线太过复杂,不当操作,对生命财产安全和自然环境有很大的风险。而微流场技术的发展使得新建化工厂具有安全,低成本,紧凑和环保等优点。微反应器中的流体通道或分散规模为微米级,微反应技术具有四个优点。一是传质和传热效率高,能准确控制反应条件,混合强度高,浪费少;二是是小通道尺寸,可以更好地控制产品形态和粒径;三是连续反应过程,提高生产效率,无批次差异;四是设备体积小,减少现场投资;该设备是静音设备,能耗低。
本课题研究了扁桃酸酯在两相不互溶溶剂中在脂肪酶催化下催化水解的最佳反应条件,并尝试使用微流场技术强化反应过程,以及进一步筛选反应条件以达到高产率,高选择性的目标。
第一章 绪论
1.1、扁桃酸
扁桃酸(又称α-羟基苯乙酸,又名苦杏仁酸、苯羟乙酸,英文名Mandelic acid CAS号:90-64-2,分子量152.15,熔点118-121℃,易溶于水、乙醇) [1],具有R、S两种构型,其中R-(-)-扁桃酸是一种重要的手性中间体,在多种药物的合成中均有广泛应用,例如用于合成青霉素和头孢拉定等抗生素、治疗水肿和风湿疾病的药物、抗肿瘤药物、血管扩张药环扁桃酸酯和农药等[2];也可作为手性试剂,拆分其它手性化合物。[3]因此,制备光学纯的手性扁桃酸在健康、农业、材料和环保等领域都具有深刻而长远的应用价值。
目前光学纯的手性扁桃酸主要由物理化学方法、化学法和生物催化法等进行合成。其中,物理化学方法主要为毛细管电泳法和色谱分离法。色谱法中主要有高效液相色谱法(HPLC)和气相色谱法(GC),[4]其中,虽然使用手性色谱柱拆分法进行合成,得到的产物纯度高,但是由于手性添加剂价格高昂,因此缺点是难以大规模的工业化生产。[5]化学法生产手性扁桃酸主要分为化学拆分法、不对称合成法和电化学法等。其中化学拆分法一般利用生物碱、手性胺等与扁桃酸形成非对映体盐结晶从而进行拆分,缺点是产品收率偏低,环境破坏大,反应条件难以控制。[6]生物方法生产光学纯扁桃酸主要有氧化还原法和水解法等。利用生物方法制备光学纯的扁桃酸具有立体、区域和化学选择性较高,并能完成一些难以用化学方法进行的反应等优点。[7]本实验采用假丝酵母脂肪酶在微流场中水解扁桃酸酯的方法制备扁桃酸,该反应具有反应条件简单温和,易满足易控制,对环境污染小等优点。
1.2,酶
酶是一种高效的生物催化剂,对比一般的催化剂来说,拥有着良好的区域选择性和空间选择性的优点,且在常温,常压,ph值中性等温和的反应条件下就能高效的发挥作用。 [8]由于反应选择性强,且高效迅速,几乎没有副反应发生,所以酶催化反应的效率比化学法催化合成反应高千万到十万亿倍。[9]避免了许多化学合成中的不足。由于酶的不对称结构,高选择性和单一性,以及在温和条件下催化反应的高效率和特异性,一些研究表明酶催化在手性化合物的合成和拆分方面具有广阔的应用前景。[10]
1.2.2酶催化在手性合物成中的应用
手性化合物广泛用于医药,农药和精细化学品,其需求日益增加。 酶催化技术由于其催化反应效率高,产物有较高的光学纯度,工艺相对简单,环境污染较小等特点,已成为制备手性化合物最重要的技术之一。[11]近年来,人们逐渐将酶运用于有机合成中,并有了较大的进展,利用酶催化反应时的强烈区域和空间选择性把反应物前体不对称化,从而得到大部分的复杂手性分子。[12]目前这种方法主要运用在有机物的不对称氧化、还原、裂解、水解(与之对应的逆反应)反应的催化上。
1.2.3 酶催化的不对称水解反应
水解反应是使用酶做生物催化剂进行手性合成的最常见反应,通过利用酶的催化特性(立体选择性)对一些脂类或者环氧化物进行水解,再纯化能够得到光学纯的异构体。[13]这些反应通常在水相发生,为了提高反应物的利用率,有时候也会选择有机溶剂,以使反应更加顺利。[14]目前,这些反应中频繁使用的酶大多是水解酶,其中最重要和常见的是脂肪酶,主要是因为它们不依赖辅酶。[15]
1.2.4脂肪酶
脂肪酶( Lipase,EC3. 1. 1 . 3)可以水解三酸甘油 酯产生脂肪酸、单甘油酯、双甘油酯及甘油,在有机溶剂(包括超临界流体)中,也可催化逆水解反应,例如酯 化、交酯化、氨解、交流酯化及肽解等反应。[16]脂肪酶已广泛应用于食品,造纸,皮革,洗涤剂,化学原料和药物合成等领域,[16]其中脂肪酶研究的焦点主要集中于药物的合成上。目前,临床常用药物中60%以上是手性药物。但是通过常规的化学方法合成手性分子是不令人满意的。[17]存在反应工艺长且繁复,容易残余作为催化剂的重金属,从而影响产率等缺点。而脂肪酶对底物具有高度的立体选择性,并且可以通过单步反应高效地制备手性产物,这使得脂肪酶在合成光学纯化合物和转化手性药物中有着独特的地位。[18]在几乎不含水的有机溶剂中,脂肪酶依然可以稳定的发挥催化作用,这让多数有机化合物的合成过程中使用了大量的非水介质的酶。随着非水酶学的建立和进步,在一些手性药物中间体的合成制备过程中,脂肪酶扮演者越来越重要的角色。与此同时,脂肪酶作为一种生物活性催化剂,具有很强的空间选择性,特别合适在通过普通的化学方法难以成功的多官能化合物的合成中使用,并且可以有效避免副产物如多取代产物的出现。[19]脂肪酶催化反应不仅具有强烈优异的立体和区域选择性,而且具有反应所需要的条件简单,环境友好等长处,可以保证产品的光学选择性和产率。脂肪酶作为一种生物催化剂为反应流程提供了更环保,更有效的方法。理论上说,基本之前能够用化学方法生产合成的药物或者中间体,都可以用酶的催化方法进行代替。当然不能也不可能完全将化学合成法排除出去,重点是哪种方法在实际应用中更加经济、高效。如何将二者巧妙的结合已成为现在生物有机合成研究中一个重要的方向,它必将对光学活性药物的合成和应用起到正面的推动作用。[20]
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: