恶唑烷酮衍生的联烯酰亚胺的合成及其反应研究毕业论文
2020-04-06 11:13:57
摘 要
1-氮杂丁二烯是一类分子结构中含有一个碳碳双键(C=C)以及一个与之共轭的碳氮双键(C=N)官能团的化合物,而且是一种多功能的参与有机(不对称)转化砌块,被广泛的应用于有机合成中的多取代化合物以及杂环化合物的合成。目前,1-氮杂丁二烯类化合物主要由α, β-不饱和羰基化合物和伯胺缩合而成,然而此类方法存在着一定局限性,需要预先合成α, β-不饱和羰基化合物,并且当反应底物为α, β-不饱和酮类化合物时,极易发生氮杂迈克尔加成反应。现有的通过炔烃/亚胺复分解的合成方法又存在着催化剂不易获得和反应适用范围小等问题。因此,发展一种条件温和,高原子经济性的1-氮杂丁二烯类化合物合成方法具有十分重要的意义。
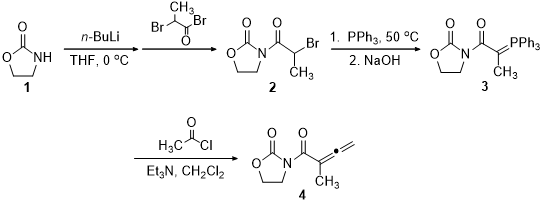
为了解决这一问题,我们设计了一种通过亚胺与联烯酰亚胺的[2 2]环加成/异构化反应合成1-氮杂丁二烯类化合物的方法。本文首先以2-噁唑烷酮为起始原料,经强碱n-BuLi拔氢并与2-溴-丙酰溴发生亲电取代得到3-(2-溴)丙酰基噁唑-2-酮,然后与三苯基膦反应制备得到叶立德试剂,叶立德试剂再与乙酰氯经wittig反应得到了噁唑烷酮衍生的缺电子联烯类化合物。采用缺电子联烯和富电子亚胺为反应原料,通过优化溶剂和催化剂,最终实现了Ni(ClO4)2·6H2O催化的[2 2]环加成/异构化反应,以92 %产率获得噁唑烷酮衍生的氮杂丁二烯类化合物。确定最佳反应条件为:以Ni(ClO4)2·6H2O作催化剂,并且与5 Å分子筛预先混合过夜,以CH2Cl2为溶剂,在室温下反应12小时。该研究结果为探究联烯酰亚胺类化合物与其它反应物的之间的反应提供了一种可行的方法。
关键词:缺电子联烯,氮杂丁二烯,环加成/异构化
Abstract
1-Azadienes bearing a carbon−carbon double bond and conjugated imino functional groups are synthetically versatile building blocks participating in a substantial class of (asymmetric) transformations, and are widely used in the synthesis of polysubstituted compounds and heterocyclic compounds in organic synthesis.The common approach to assemble 1-azadienes is mainly considered by means of condensation of α, β-unsaturated carbonyls and primary amines. This method requires the preformation of α, β-unsaturated carbonyls and usually suffers from the undesired aza-Michael addition reaction, especially with α, β-unsaturated ketones. The existing alkyne/imine metathesis strategy suffered from very limited scope and unusual catalyst system. Therefore, a simple reaction protocol with high atom economy under mild condition remains lacking and highly desirable.
In an effort to address the issue as mentioned above and create a conceptually unprecedented paradigm of catalytic [2 2] cycloaddition/isomerization of imines for 1-azadienes, we turned our attention to investigate the reaction by using allenes and imines. Oxazolidin-2-one was first used as the starting material, then 3-(2-bromopropanoyl)oxazolidin-2-one was synthesized by strong base n-BuLi dehydrogenation and electrophilic substitution with 2-bromo-propionyl bromide, and then reacted with triphenylphosphine to prepare Ylide reagent. Witiig reaction with acetyl chloride was carried out to give electron deficient allene compounds derived from oxazolidinone. Optimizing the solvent and catalyst, the [2 2] cycloaddition/isomerization reactions of electron-deficient allene and electron-rich imine were realized. Finally, azadienes derived from oxazolidinone were obtained at the yield of 92 %. The optimum reaction conditions were determined as follows: Ni(ClO4)2·6H2O was used as catalyst and was premixed with 5 Å molecular sieve overnight, and CH2Cl2 was used as solvent for 12 hours at room temperature. The results provide a feasible method for exploring the reaction between ienimide and other reactant.
Key Words:Electron-deficient allene, Azadienes, cycloaddition/isomerization
目录
第1章 绪论 1
1.1 联烯类化合物简介 1
1.2 噁唑烷酮衍生物的简介 4
1.3 氮杂丁二烯类化合物的简介 5
1.4 联烯类化合物的环加成反应 6
1.4.1 联烯类化合物[4 2]环加成反应 7
1.4.2 联烯类化合物[3 2]环加成反应 9
1.4.3 联烯类化合物[2 2]环加成反应 10
1.5 本论文研究意义及立题思想 12
第2章 实验部分 13
2.1 噁唑烷酮衍生的联烯酰亚胺的合成 14
2.1.1 合成路线 14
2.1.2 3-(2-溴)丙酰基噁唑-2-酮的合成 14
2.1.3 3-(2-三苯基磷代)丙酰基噁唑-2-酮的合成 15
2.1.3 3-(2-甲基-2,3-二烯)丁酰基噁唑-2-酮的合成 15
2.2 富电子亚胺的合成 16
2.2.1 3-乙烯基吲哚的合成 16
2.2.2 N-亚苄基-1-苯基甲胺的合成 16
2.2.3 N-亚苄基-2-甲氧基苯胺的合成 17
2.3 噁唑烷酮衍生的联烯酰亚胺与亚胺的反应研究 17
2.3.1 噁唑烷酮衍生的联烯酰亚胺与N-亚苄基-2-甲氧基苯胺的反应 17
2.3.2 噁唑烷酮衍生的联烯酰亚胺与N-亚苄基-1-苯基甲胺的反应 19
2.3.3 噁唑烷酮衍生的联烯酰亚胺与3-乙烯基吲哚的反应 19
2.4 本章小结 19
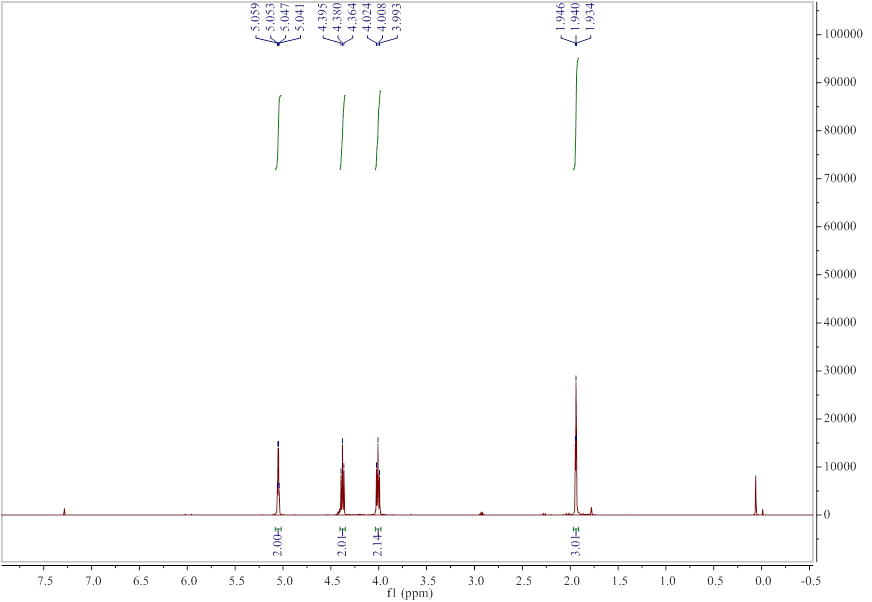
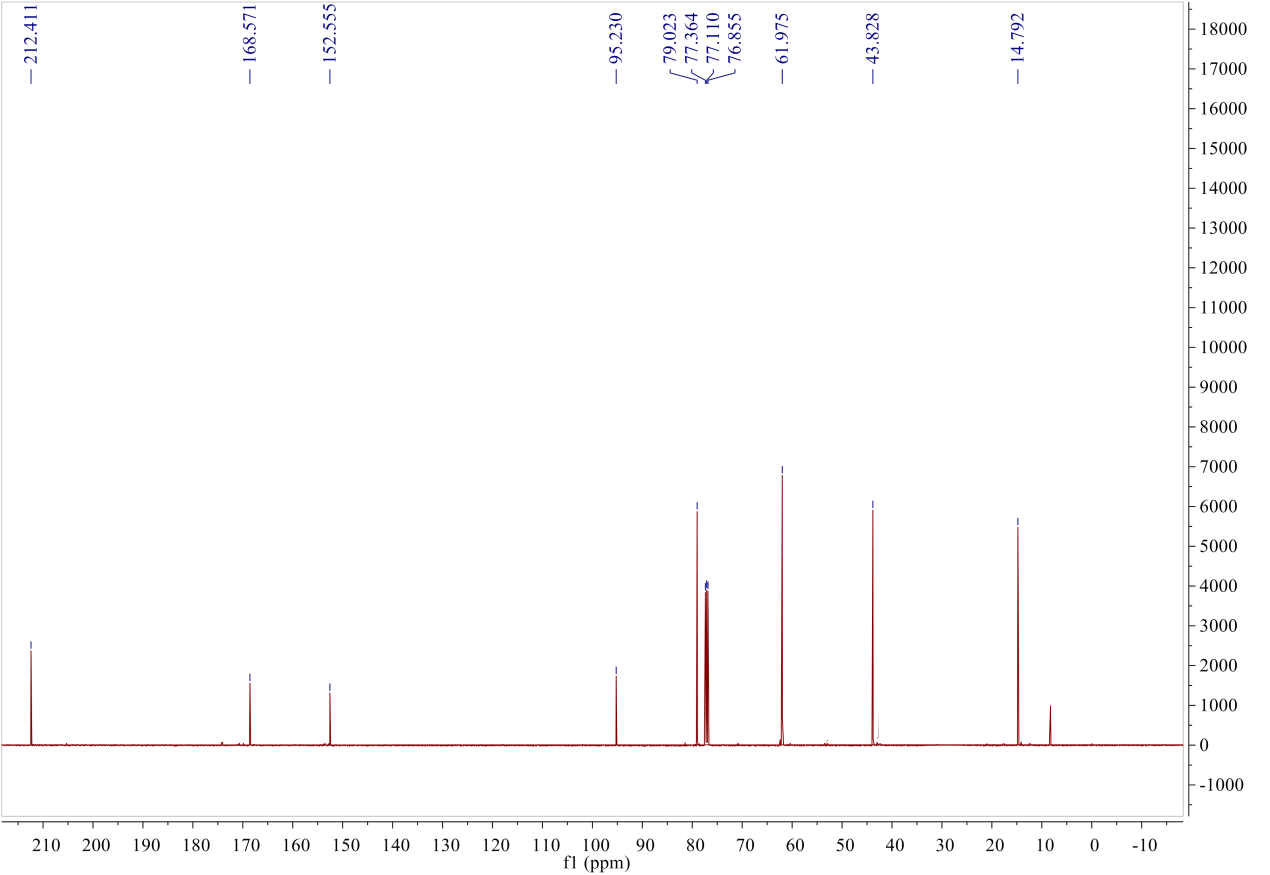
2.5 核磁数据附图 21
参考文献 27
致谢 29
第1章 绪论
1.1 联烯类化合物简介
联烯又称累积二烯,是一类含有1,2-二烯官能团(丙二烯结构)的化合物。联烯1,2-二烯官能团中两端的α, γ-碳原子均采用sp2杂化,中间的β-碳原子采用sp杂化,其未参与杂化的两个相互垂直的p轨道分别与α, γ-碳原子中未参与杂化的p轨道重叠而形成两个相互垂直的π键(图1.1)。由于连续两个相互垂直的π键结构特殊、性质活泼,让联烯类化合物具有多个反应位点。通过在1,2-二烯官能团两端引入吸电子或给电子取代基团,可以调控联烯官能团上的电子云密度,从而控制联烯类化合物的反应位点。

图 1.1 联烯类化合物的结构
早在1887年Burton和Pechmann[2]就制备出了第一个联烯类化合物,但是直到1954年,Jones[3]才确定了该联烯的结构。联烯化合物是许多天然产物合成路线中具有高价值的合成前体[4],很长一段时间,人们都错误地夸大了1,2-二烯体系的不稳定性,认为联烯类化合物在化学上难以合成。所以那时Buton和Pechmann[2]首次合成联烯类化合物引起了不小的轰动。事实上,联烯化合物在自然界中早有稳定的存在。近年,许多含有1, 2-丙二烯结构的天然联烯化合物成功地被提取,并且化学家们已成功地鉴定其结构。时至今日,已有数百种含有1, 2-丙二烯结构的天然联烯化合物被发现[5]。如Pannacene[6],Mycomycin[7],Grasshopper ketone[8]等(图1.2)。
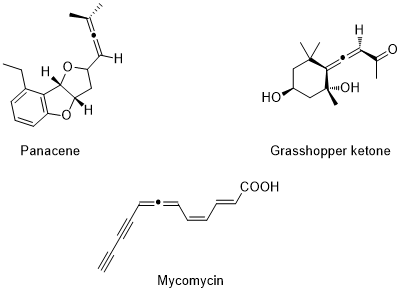
图 1.2 部分天然联烯化合物
2012年,朱灿[9]课题组通过金属催化剂钯,实现了碘代吲哚和联烯基铟试剂之间的偶联反应,如图1.3,反应中间体经过8π电环化反应,可以构建出吲哚并八元环化合物A1,以此为原料,再经过一系列反应流程即可制备出治疗抑郁症的药物分子A2。
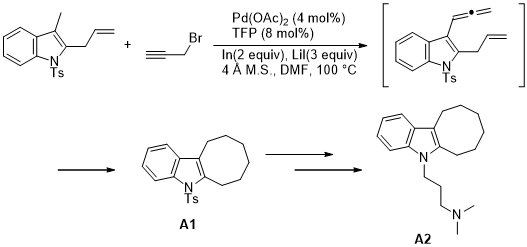
图 1.3 碘代吲哚和联烯基铟试剂之间的偶联反应
该课题组还实验出邻碘苯胺和溴代烯炔A3在与上文反应相似的条件下也能发生偶联反应,从而制备出烯丙基取代的吲哚类化合物A4,A4再经过几步反应可合成非萜类消炎药A5(图1.4)[10]。
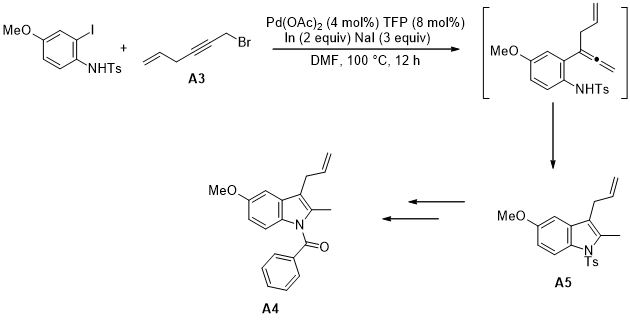
图 1.4 邻碘苯胺和溴代烯炔的偶联反应
如图1.5所示,A9是一类具有消炎以及抗肿瘤活性的天然化合物。2009年,Kris[11]小组在三苯基膦的条件下用光学活性烯酮类化合物A6与联烯酸酯进行[3 2]环加成反应,从而高效快捷地构建了化合物A7,A7再经过一系列后续反应转化得到化合物A8,而化合物A8作为天然产物A9的合成前体,对II型糖尿病也有良好的治疗效果。
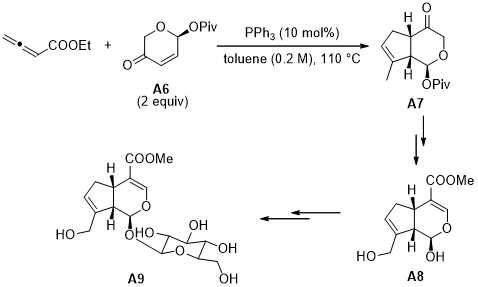
图 1.5 光学活性烯酮类化合物与联烯酸酯的[3 2]环加成反应
CRTH2是一种通过诱导辅助T细胞的而促进炎症的发病的化学引诱物同源受体分子。罗氏公司的一系列研究发现,化合物A10作为一种受体拮抗剂,其具对CRTH2具有良好的药物拮抗作用。2013年,该公司将化合物A10的合成路线优化为八步,总收率可达53 %(图1.6)[12]。
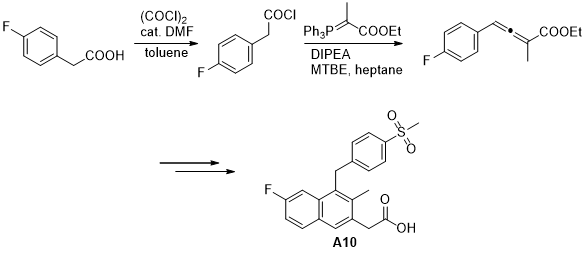
图 1.6 CRTH2拮抗剂的部分合成路线
1.2 噁唑烷酮衍生物的简介
2-噁唑烷酮及其衍生物(图1.7)是有机合成中非常重要的一类化合物,根据噁唑环或N原子上连接的不同基团,2-噁唑烷酮的衍生物主要有:2-噁唑烷酮含硝基咪唑类,N-乙烯基-2-噁唑烷酮类,5-羟甲基-2-噁唑烷酮类,5-苯乙基-2-噁唑烷酮类,4-烷氧基羰基-2-噁唑烷酮类等[13]。它们在精细化工领域都有着广泛的运用。
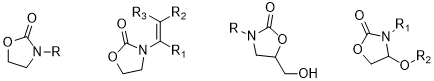
图 1.7 部分噁唑烷酮衍生物结构
2-噁唑烷酮常用在纤维,化妆品以及活性染料等化工产品中,在精细有机合成中也是卡氮芥,环己亚硝脲等化合物的重要合成中间体。它还可以用于吸收废气中的SO2气体,并通过再生循环使用。
噁唑烷酮衍生物在化工,生物,医药领域都有着广泛的应用,N-乙烯基-2-噁唑烷酮类化合物广泛应用于纤维,塑料,胶粘剂的合成,同时也是纺织助剂,染料的重要合成中间体;5-苯乙基-2-噁唑烷酮类化合物可用于合成松弛肌肉,止痛消炎类药物,2-噁唑烷酮含硝基咪唑类化合物主要用于医疗领域中作化学敏感剂和放射敏感剂,4-烷氧基羰基-2-噁唑烷酮类则常作为有机农药,医药的原料和中间体,5-羟甲基-2-噁唑烷酮类可用于合成抗菌药物,以及治疗行为紊乱的药物[13]。
1.3 氮杂丁二烯类化合物的简介
1-氮杂丁二烯类是指分子中含有一个碳碳双键(C=C)以及一个与之共轭的碳氮双键(C=N)官能团的化合物[14]。由于氮原子的诱导效应,碳氮双键的电子云偏向氮原子,导致氮杂丁二烯结构的性质完全不同于全碳的丁二烯结构(图1.8)。

图 1.8 氮杂丁二烯类化合物结构
氮杂丁二烯类化合物是一类重要的有机合成中间产物,它可以进行Diels-Alder反应,共聚反应,亲核加成反应和电环化交换反应,被广泛的应用于有机合成中的多取代化合物以及杂环化合物的合成[15]。特别是近年来氮杂丁二烯光化学反应的相关报道越来越多,由于其光化学反应的种种优越性而引起了广大化学家的重视。
上世纪七十年代,人们就开始了对氮杂丁二烯类化合物的研究。四十年来,氮杂丁二烯类化合物的合成及反应研究一直都是化学界的热点。由于该类化合物的Diels-Alder反应在天然产物合成方面的巨大潜力,Diels-Alder反应成为了氮杂丁二烯类化合物反应中报道最多的一种反应。氮杂丁二烯类化合物与亲电的亲双烯体反应比全碳的丁二烯类化合物与亲双烯体的反应要相较困难[16]。因此,要使氮杂丁二烯类化合物顺利进行Diels-Alder反应,通常在亲电的二烯体分子中连上强的给电子基团。另一方面,氮杂二烯类化合物的不稳定性和分离提纯方面的困难也是化学家们在氮杂丁二烯类化合物的反应研究中需要克服的难题。
多取代喹啉衍生物是抗癌以及抗疟疾药物的合成中重要的底物和中间体。1970年,J. Glinka[17]首次从1-烷氧基-4-芳基氮杂丁二烯出发,经一步光化学反应得到了喹啉衍生物。此后,以氮杂丁二烯为原料通过光化学合成喹啉衍生物的反应更是层出不穷。化合物A11在强碱的存在下与卤代烷反应可生成3位烷基取代的氮杂丁二烯A12,A12经一步光化学反应即可生成3烷基取代的喹啉A13(图1.9)。
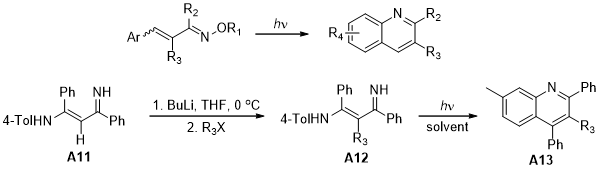
图 1.9 氮杂丁二烯的光化学反应
如图1.10所示,氮杂丁二烯类化合物与亲二烯体发生HAD([4 2]环加成)反应生成哌啶酮衍生物,穆小静等[18]用环己酮作为亲二烯体,在Lewis酸的催化下探究氮杂丁二烯的HDA反应及其单分子环合反应,其中合物A14是合成抗抑郁药文拉法星的关键步骤之一。
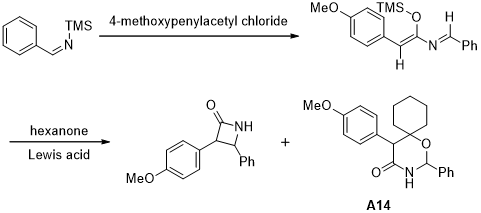
图 1.10 氮杂丁二烯的单分子环合反应及其与环己酮的HDA反应
1.4 联烯类化合物的环加成反应
环加成反应是不饱和分子间经由π键断裂成键的过程相互加成,最终得到环状产物的反应。这种合成反应以一种简便快速的方法高效的构建出复杂的分子结构,具有底物多样性,高的原子经济性,较高的化学选择性和较优良的对应选择性。因此,通过环加成反应来构建碳环与杂环骨架一直以来都是有机合成领域中的一个研究热点。
由于联烯类化合物的独特结构,自联烯类化合物结构首次测定之后,关于联烯及其衍生物的研究引起了国内外广大化学工作者的兴趣,特别是对有联烯类化合物参与的合成各种环状化合物的反应进行了大量研究,近些年来,随着人们对于联烯类化合物有了进一步深入的了解与研究,在构建碳环和杂环化合物时,联烯类化合物的环加成反应展现出了其特有的优势。
联烯类化合物因其特殊结构存在多个活性反应位点,通过改变丙二烯结构两端的取代基,可以实现联烯类化合物自身或与其他化合物间发生不同的环加成反应。如[4 2]环加成,[3 2]环加成,[2 2]环加成,[1 2 2]环加成,[2 2 2]环加成,[4 3]环加成以及[4 2 2]环加成反应等,接下来文章主要选取前三种更为常见的环加成反应进行介绍。
1.4.1 联烯类化合物[4 2]环加成反应
2011年,Matsubara等[19]报道了丙二烯A15与α, β-不饱和醛酮类化合物的[4 2]环加成反应(图1.11),该反应以Ni(cod)2作为催化剂,1,4-二氧杂环己烷作为溶剂,以三苯基膦衍生的亚胺类化合物A16作为配体,在100 oC条件下进行。在最佳配体A16存在时,α, β-不饱和醛酮类化合物容易与零价Ni发生环氧化反应,而该反应可以促进α, β-不饱和醛酮类化合物与丙二烯之间发生分子间偶极环加成。当丙二烯类化合物为单取代时,反应可以取得良好到优秀的产率(84%~99%)。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: