碳包覆钴锌双金属氧化物复合材料的合成及其作为负极在锂离子电池中应用毕业论文
2020-03-22 14:04:06
摘 要
锂离子电池因具有工作电压高、无记忆效应、自放电小、比容量大、循环稳定性好、污染小等一系列的优点,吸引了广大学者的关注,是具有广阔发展前景的便携式新型化学电源。由于传统的锂离子电池(以钴酸锂为正极,石墨碳为负极)本身较低的比容量,也很难在制备工艺方面得到较大突破。因此,人们对锂离子电池的研究方向开始转变,越来越倾向于新型电极材料的开发与应用之上。
相较于传统的石墨碳负极,过渡金属氧化物因为具有比较高的理论比容量而备受关注。但是在充放电循环中,这种类型的材料的体积会产生较大变化从而降低了电池的性能,所以需要进一步的研究。其中,最受欢迎的便是氧化锌。本文采用溶剂热的方法合成了掺钴锌的MOF-74(MOF-74-ZnCo)。在氩气气氛下,通过MOF-74-ZnCo的热处理,得到了CZO@C复合材料,并对材料进行XRD、XPS、氮气等温吸附表征;将其制成实验电池后进行了电化学性能的测试。测试结果表明:经过200圈循环后,CZO@C电极材料的比容量为394.4mAh/g,虽然容量不是很高,需要深入研究,但是循环稳定性能良好,在倍率测试中也展现了优异的可逆性。
关键词:锂离子电池;负极材料;氧化锌;掺杂
Abstract
Li-ion batteries have attracted the attention of many scholars because of their advantages such as high working voltage, no memory effect, small self-discharge, large specific capacity, good cycle stability, little pollution and so on. It is a new portable chemical power supply with broad development prospects. Because of the low specific capacity of the traditional lithium ion battery (lithium cobalt as positive electrode, graphite carbon as negative electrode), it is difficult to make a great breakthrough in the preparation process. Therefore, the research direction of lithium-ion battery is changing, and it is more and more inclined to the development and application of new electrode materials.
Compared with the traditional graphite carbon anode, transition metal oxides have attracted much attention because of their high theoretical specific capacity. However, in charge / discharge cycle, the volume of this type of material will change greatly, which will reduce the performance of the battery, so further research is needed. Among them, the most popular is zinc oxide. In this paper, MOF-74 MOF-74-ZnCoO doped with cobalt and zinc has been synthesized by solvothermal method. The CZO@C composites were prepared by heat treatment of MOF-74-ZnCo in argon atmosphere, and were characterized by isothermal adsorption of CZO@C and nitrogen. The electrochemical performance of the battery was tested. The test results show that the specific capacity of CZO @ C electrode material is 394.4 mAh / g after 200 cycles. Although the capacity is not very high, it needs further study, but the cycle stability is good, and it also shows excellent reversibility in the rate test.
Keywords: Lithium ion battery; Anode material; Zinc oxide; Cobalt doping.
目 录
摘要 I
Abstract II
第1章 绪论 1
1.1引言 1
1.2 锂离子电池简介 1
1.2.1锂离子电池的发展历程 1
1.2.2锂离子电池的构成 2
1.2.3锂离子电池的工作原理 5
1.2.4锂离子电池的特点及发展趋势 5
1.3锂离子电池负极材料研究现状 7
1.3.1碳素类材料 7
1.3.2合金类材料 7
1.3.3过渡金属氧化物 8
1.3.4 其它负极材料 8
1.4 金属有机框架 8
1.5课题研究意义 8
第2章 实验部分 10
2.1实验药品及仪器设备 10
2.1.1实验药品 10
2.1.2 实验仪器 11
2.2 碳包覆钴锌双金属氧化物材料的制备 11
2.3 材料物理性质的表征 12
2.3.1 X射线衍射分析(X-ray diffraction, XRD) 12
2.3.2 扫描电子显微镜(Scanning Electron Microscope, SEM) 12
2.3.3 X射线光电子能谱(X-ray Photoelectron Spectroscopy,XPS) 12
2.3.4氮吸附测试 12
2.4 材料化学性能的表征 12
2.4.1 电极制备 12
2.4.2 实验电池的组装 12
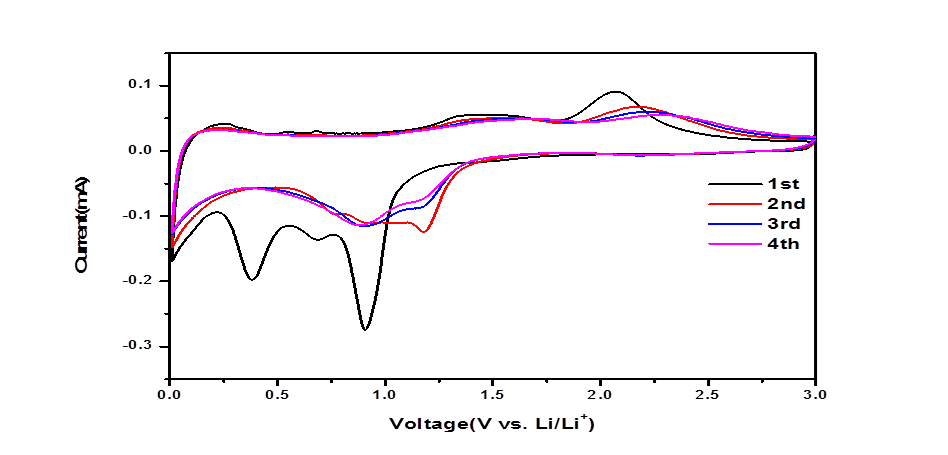
2.4.3 循环伏安测试(CV) 13
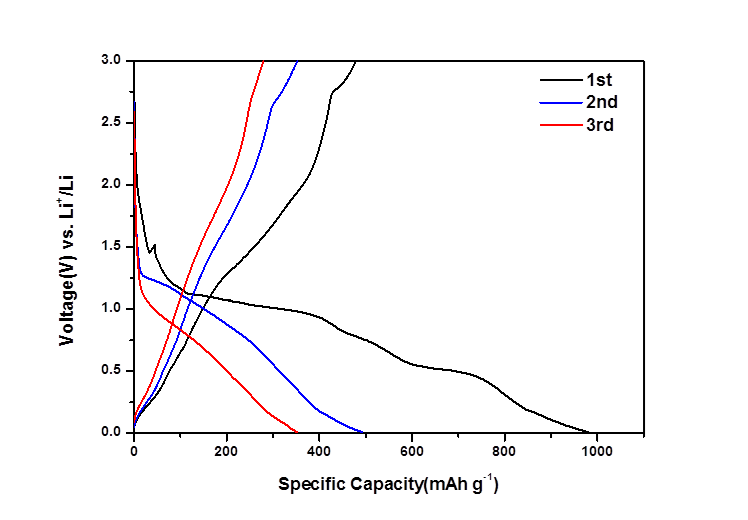
2.5.2 恒流充放电测试 13
2.5.3 电化学交流阻抗测试 13
第3章 结果与讨论 14
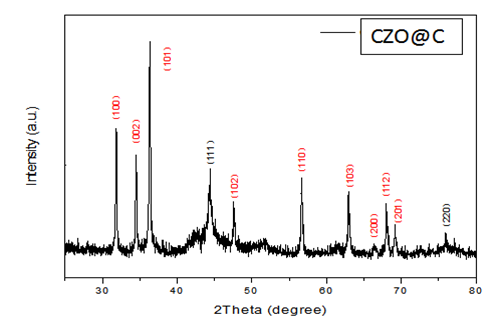
3.1 XRD测试 14
3.2形貌分析 16
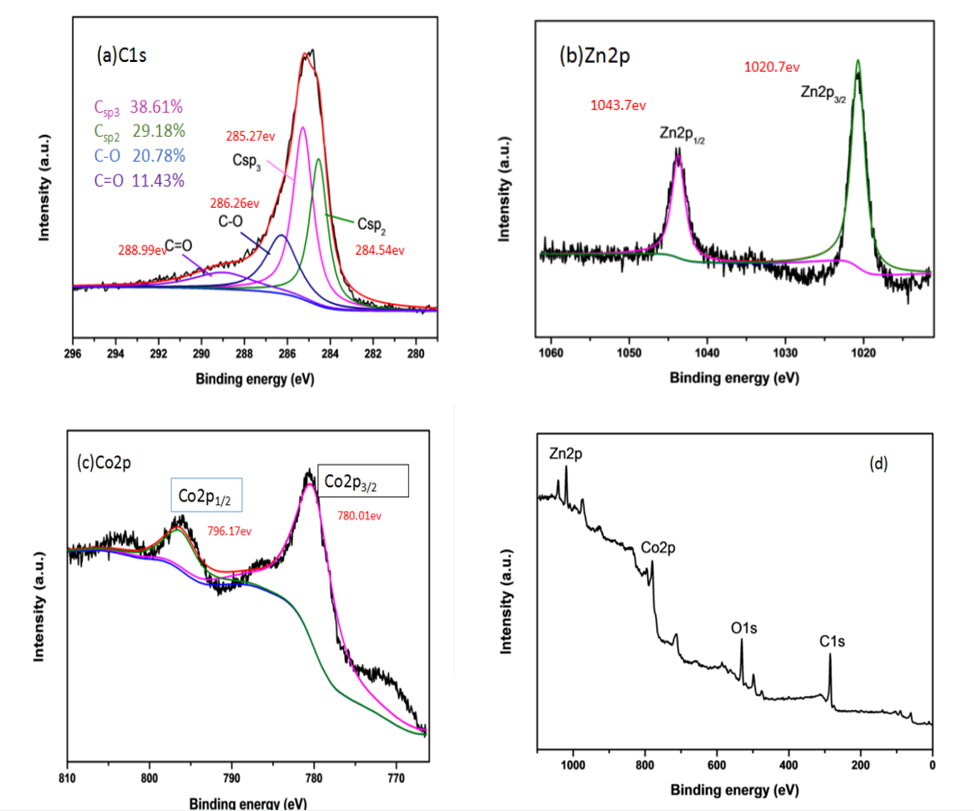
3.3 XPS测试 17
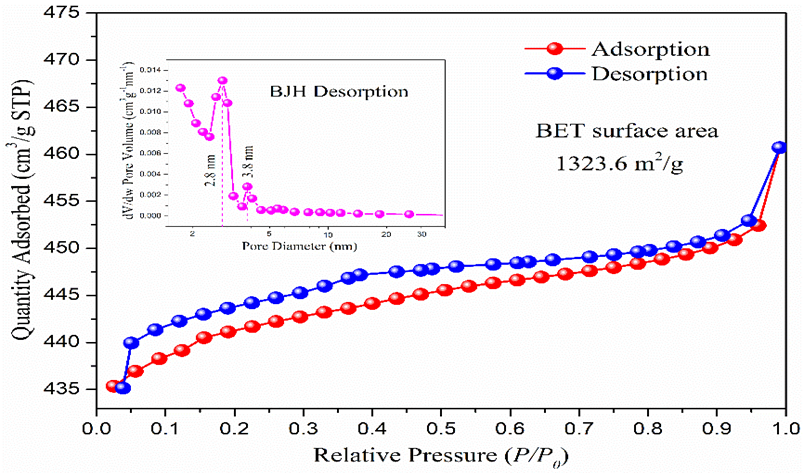
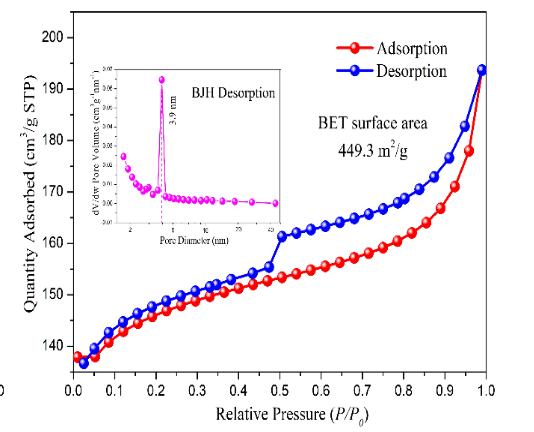
3.4 氮吸附 18
3.5 电化学性能测试 20
第4章 结论 24
参考文献 25
致谢 26
第1章 绪论
1.1引言
绵延几千年的人类社会发展史,不仅仅是科技文明的进步史,却也是资源耗竭、平衡崩塌、环境污染的血泪史。为保证社会经济的可持续发展,环保可再生的新型清洁能源日益引起世界各国的关注。在众多新能源中,锂离子电池由于能量密度高,体积小、使用寿命长,质量轻、安全可靠、无记忆效应、对环境无公害等,受到了广泛应用,是当今科研人员的研究热点。
在日常生活中,锂离子电池已被广泛应用到手机、手电筒、笔记本、平板等各类便携式电子设备中,未来也注定成为电动汽车、飞机、人造卫星等现代高科技的重要化学电源。因此,研发和制备电池关键材料提高电池性能,适应和促进时代发展潮流是大势所趋,更是历史必然。
1.2 锂离子电池简介
1.2.1锂离子电池的发展历程
意大利人伏特(Volt)可以说是电池的鼻祖了,1800年,发明了人类历史上第一套电源装置,打开了电池世界的大门,他也因此获得了伯爵的头衔,人们为了纪念他,将电压的单位定为伏特。接下来,随着科研人员的不断探索研究,铅酸电池、氯化银电池、镍镉电池、镍氢电池、锂电池等一系列电池逐渐开始出现并深入人类的生活中。
锂电池是指以锂金属作负极材料的电池。锂为碱金属,原子量仅有6.94,熔点为181.5℃,由于电化学当量最小(0.26 g/Ah)、质量最轻及标准电极电位最负(-3.045 V),因此理论上锂离子电池具有相当大的能量密度。
20世纪50年代,由于石油危机的爆发迫使人们寻找替代能源,由于锂突出的自身优势,受到了研究者的关注,锂电池开始被研究。1958年,Harris提出使用有机电解液充当电解液的这一想法使得锂离子电池研究取得一定进展。1972年,埃克森的M.S.Whittingham成功研制出以金属锂作为负极材料的电池,自此,世界上第一个锂电池问世。1977年,Michel Armand首次提出用嵌锂化合物代替二次锂电池中的金属锂负极,在充放电过程中,此类化合物可以进行可逆的Li 的嵌入和脱出,即“摇椅式电池”构想。也是同一年,锂离子电池的雏形也因Goodenough J提出将钴酸锂用作锂离子电池正极材料而形成。1985年,发现锂电池的负极材料可以使用碳材料来充当。直至二十世纪八十年代末,日本索尼(Sony)公司以嵌锂焦碳为负极活性物质,以过渡金属氧化物作正极材料,制备出了具有良好循环性能、较高电压的高比能量的电池,并且首次提出了“锂离子电池”这一概念。1990年2月,索尼公司正式向市场推出了第一款以碳材料为负极、以含锂化合物为正极的商用锂离子电池[1]。锂离子电池由于其优越的性能,被迅速应用于手机、电脑、电动汽车、导弹等个领域,彻底革新了电子产品的面貌,也成为日常生产生活不可分割的一部分。
1.2.2锂离子电池的构成
锂离子电池主要由隔膜、电解液、正极和负极四部分构成。
1.2.2.1锂离子电池的隔膜
隔膜是锂离子电池内部重要组成部分。需要满足以下要求:
(1)为确保锂离子在正负极之间脱嵌的正常进行,所以材料需要有一定的孔径;
(2)隔断正负极的同时具有良好的导电性;
(3)化学和电化学性能稳定,不被电解液腐蚀;
(4)与电解质溶液有良好的韧性。
最常见的主要是聚丙烯(PP)、聚乙烯(PE)、或者两者组成的二层隔膜或和三层隔膜。锂电池研发初期主要使用聚丙烯材料充当隔膜,主要由于其电化学稳定性较好、韧性良好、价格低廉。Celgard 2300,是实验室主要使用的一种三层隔膜。
1.2.2.2 锂离子电池的电解液
电解液是锂离子电池的重要组成部分,在正负电极之间起着传输离子和传导电流的作用,影响着电池的容量、循环寿命和工作温度。良好的电解质体系应具备的特点有:
(1)锂离子电导率高;
(2)良好的热稳定性和化学稳定性,不与电极材料隔膜等发生反应;
(3)安全、无毒、成本低等特点。
最常用的电解液体系有1M LiPF6/EC-DMC, 1M LiPF6/EC-DEC, 1 M LiPF6/PC-DEC、 1M LiPF6/PC-DMC。下表给出了常用有机电解液体系的组成。
表1.1电解液组成
电解液 | 电解质 | 六氟磷酸锂(LiPF6)、高氯酸锂(LiCl04)、四氟硼酸锂(LiBF4)、三氟甲基磺酸锂(LiCF3SO3)等[20]。 |
溶溶剂 | 碳酸脂类:碳酸乙烯酯(EC)、碳酸丙烯酯(PC)、碳酸二甲酯(DMC)、碳酸二乙酯(DEC)等[20]。 醚类有机溶剂:四氢吠喃(THF)、二甲氧基甲烷(DMM)、1,2一二甲氧基乙烷(DME)、 2一二甲氧基丙烷(DMP)[20]。 羧酸脂类:丁酸甲酯(MB)和丁酸乙酯(EB)[20]。 |
1.2.2.3锂离子电池的正极
正极是电池的重要成分。在充放电过程中,要提供电池正常脱嵌所需的锂,所以一般是锂嵌入化合物。需要具备要求如下:
(1)拥有较高的氧化还原电位,从而得到更高的输出电压;
(2)能够允许大量的锂离子嵌入和脱出从而得到更高的比容量;
(3)材料在锂离子嵌入和脱出的过程中能够保持结构稳定,从而保证电池拥有良好的循环性能;
(4)在充放电过程中,化学性能稳定,不与电解质等发生反应;
(5)有较好的离子和电子电导率,减少电极极化,并且能够进行大电流放电;
(6)价格便宜,安全,绿色,环保。
常用的正极材料如下表1.2所示,基于表上所展示的优缺点,钴酸锂是最受欢迎的正极材料。
表1.2常用离子电池正极材料
材料 | 比容量/(mAh/g) | 工作电压/(V) | 优点 | 缺点 |
钴酸锂 | 155 | 3.88 | 工作电压高,不可逆容量小,离子电子电导率良好 | 放电比容量低 循环稳定性差 成本较高 |
镍酸锂 | 200 | 3.55 | 成本低 | 受热易分解稳定性较差 |
锰酸锂 | 120 | 4.00 | 成本低、污染小 | 可逆容量低 |
磷酸亚铁锂 | 160 | 3.4 | 循环性能好 | 难合成 |
1.2.2.4锂离子电池的负极材料
负极也是电池的重要部件。应满足以下特点:
(1)氧化还原电位要尽可能的低(接近金属锂)以增大电池的输出电压;
(2)允许大量锂的嵌入和脱出以得到较高的容量;
(3)在锂的嵌入和脱出中保持结构稳定,从而保证电池拥有良好的循环性能;
(4)有较好的电子导电率和离子导电率,减少极化;
(5)不和电解质反应;
(6)安全、环保、资源丰富、价格低廉。
目前而言,没有同时满足以上要求的负极材料。金属锂容易形成锂枝晶,合金会引起体积膨胀,碳素类材料比容量较低。目前,锂离子电池商业化负极材料主要是碳素类材料。
1.2.3锂离子电池的工作原理
锂离子电池简单来说就是锂离子的浓差电池。电池所使用的正、负极材料的活性物质是能够可逆地嵌入与脱出Li 的具有层状或者隧道结构的物质。锂离子电池主要是在和外电路连通以后,充电时,锂离子从正极脱出嵌入负极,同时电子从外电路补偿到负极。放电时相反,锂离子在正极和负极之间来回移动实现运转。下面为工作原理示意图。
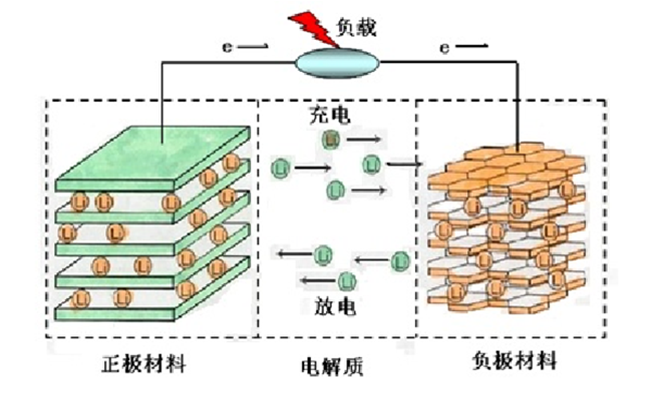 图1.1锂离子电池工作原理图
图1.1锂离子电池工作原理图
以钴酸锂( LiCo02)为正极,碳材料为负极这一典型锂离子电池电池为例。在充电时,钴酸锂失去电子,从Co3 变为Co4 ,Li 从钴酸锂晶格中脱出,经由电场提供动力,电解液对离子的传输作用通过隔膜,最终嵌入石墨炭层中,形成了锂碳层间化合物(LixC6)。在放电时,锂碳化合物失去电子,Li 从石墨碳层脱出,经电场的驱动,电解液的输送,通过隔膜进入钴酸锂正极,钴酸锂得到电子还原为三价。
石墨碳/钴酸锂电池的电极反应和电池反应如下:
负极:6C xLi xe-=LixC6
正极:LiCoO2=Li1-x Co2 xLi xe-
电池总反应为:LiCoO2 6C= Li1-x CoO2 LixC6
1.2.4锂离子电池的特点及发展趋势
相比于之前广泛使用的二次电池铅酸电池、镍镉电池和镍氢电池等,锂离子电池在某些性能方面具有一定的优势,为了更形象地表示出与传统二次电池铅酸电池、镍镉电池和镍氢电池的区别,表1.3展示了常用电池的性能对比图。
表1.3常用二次电池对比图
电池类型 | 功率密度/(W/kg) | 能量密度 /(W• h/kg) | 单元电压/(V) | 循环寿命/(次) | 成本/($/kWh) | 环境保护 | 自放电(%) | 记忆效应 |
铅酸电池 | 200-300 | 35-40 | 2.0 | 300-500 | 75-150 | 污染 | 6 | 无 |
镍镉电池 | 150-350 | 40-60 | 1.2 | 500-1000 | 100-200 | 污染严重 | 25-30 | 有 |
镍氢电池 | 150-300 | 60-80 | 1.2 | 500-1000 | 230-500 | 无污染 | 30-35 | 无 |
锂离子电池 | 250-450 | 90-160 | 3.6 | 600-1200 | 120-200 | 无污染 | 6-9 | 无 |
纵观锂离子电池的优点和缺点,表格充分表现出来锂离子电池相较于其它电池优良的性能,具体表现在以下几个方面:
- 能量密度高:能量密度明显高于其它二次电池。
- 电池工作电压高:锂离子电池相对于其他常见的三种电池,工作电压是它们的2-3倍左右。
- 循环寿命长:相比于传统二次电池有一定程度程度的延长。
- 自放电率较小:第一圈充放电时,锂离子电池负极表面形成的固体电解质膜较好地防止了自放电。
- 无记忆效应:在使用锂离子电池时,由于其没有记忆效应,所以可以随时进行充放电的操作,不需要必须把内部的电量全部使用完后,才可以进行充电操作,这给日常的使用带来一定的方便。
- 环境污染小:相较于传统二次电池,锂离子电池的材料不含有铅、汞等有毒物质,污染小。
这些优于传统电池的性能都决定了锂离子电池注定成为研究的热点。虽然相比较于传统二次电池锂离子电池具有一定的优越性,但仍然存在某些缺点或不足,具体表现在:
(1)内部阻抗大:因为锂离子电池的电解液是有机溶剂,导电率要低于其他几种电池,所以阻抗远远大于其他传统二次电池。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: