四氧化三铁磁珠富集回收污水中重金属离子铬酸根的研究毕业论文
2020-02-19 14:35:33
摘 要
Fe3O4磁性纳米粒子是一种具有发展潜力的吸附剂,在污水处理中因其超顺磁性、表面效应及高生物相容性等特性展现出广阔的应用前景。本文拟合成Fe3O4磁珠并对其去除溶液中Cr(VI)的因素影响及吸附机制进行研究。
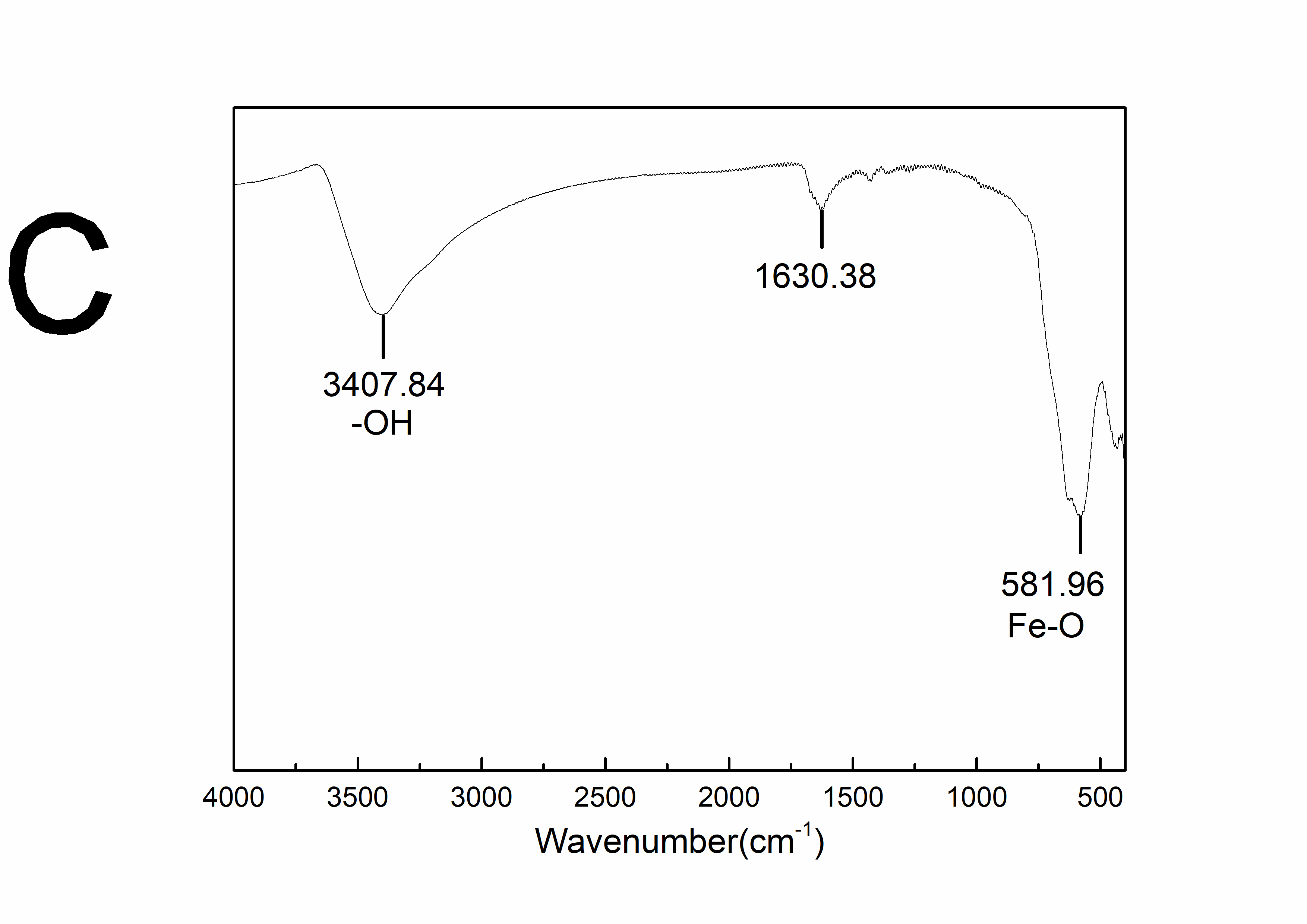
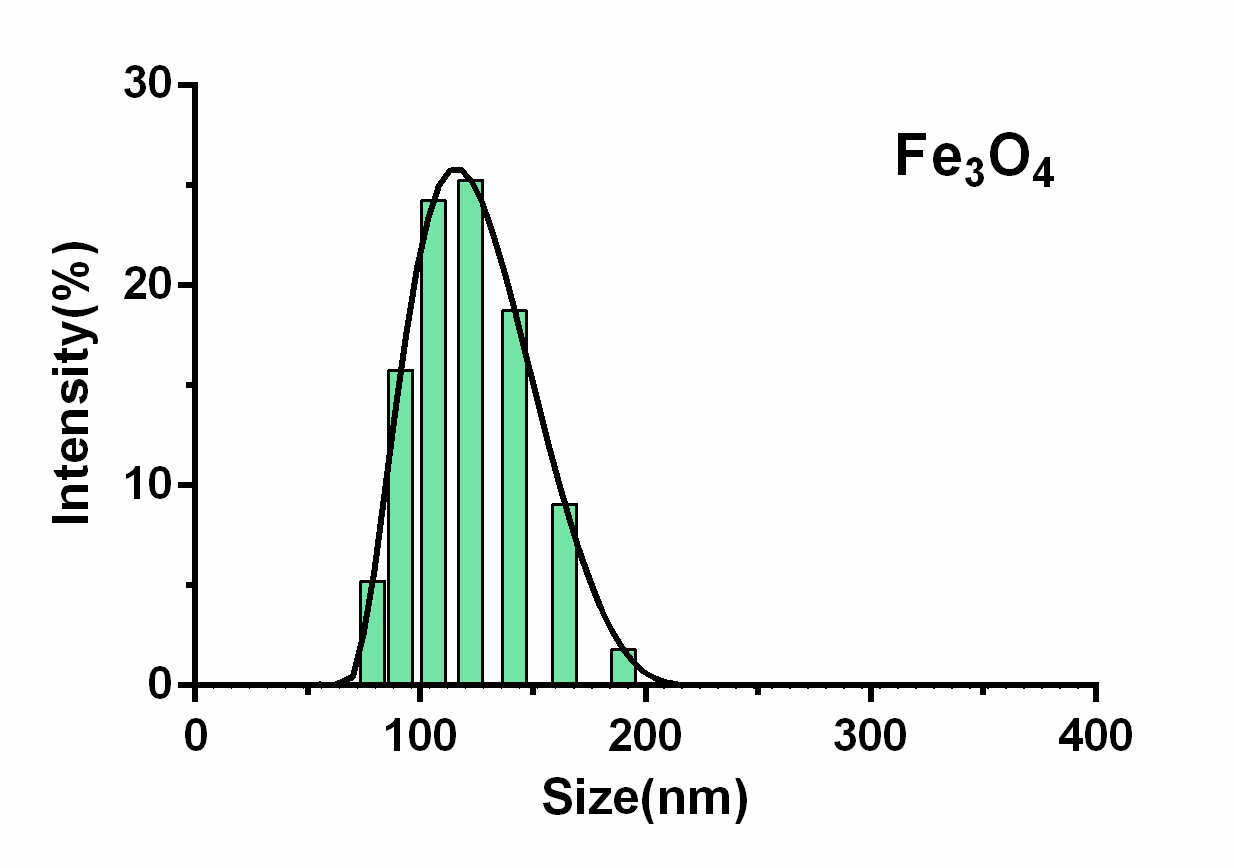
利用共沉淀法制备Fe3O4磁珠,采用傅里叶红外光谱法(FT-IR)、透射电子显微镜法(TEM)、粒径分布分析(PSD)、磁性观测分析对其进行结构成分、形貌及磁性的表征。最终合成的磁珠在581.96cm-1处有Fe-O键的特征吸收峰,在3407.84cm-1处出现较宽的-OH伸缩振动峰,平均水合粒径为111.8nm,具有良好的超顺磁性。利用制备的Fe3O4磁珠系统地研究了吸附时间、Fe3O4磁珠用量、Cr(VI)初始浓度、pH、温度对Cr(VI)吸附效果的影响。各因素影响效果由大到小依次为pH、温度、Cr(VI)初始浓度和吸附时间。用准一级和准二级模型拟合吸附动力学曲线,吸附数据更符合准二级动力学模型,R2达0.9964,表明以化学吸附为主。采用Langmuir和Freundlich吸附等温线模型描述平衡数据,Langmuir模型能较好描述Cr(VI)在Fe3O4磁性纳米颗粒上的吸附,R2达0.9902。此外,研究了盐离子浓度及种类对吸附的影响,结果表明盐离子浓度对吸附影响不大,Mg2 提高去除率的效果较明显,而SO42-则使去除率降低。
关键词:污水处理,Fe3O4磁珠;Cr(VI);吸附
Abstract
Fe3O4 nanoparticles are promising potential adsorbents and exhibited remarkable application prospects for wastewater treatment due to its superparamagnetism, surface effect and high biocompatibility. In this paper, Fe3O4 magnetic nanoparticles were synthesized to study the factors affecting Cr(VI) removal and adsorption mechanism during the process.
Fe3O4 nanoparticles were synthesized by chemical co-precipitation method. Its structure, composition, morphology and magnetism were characterized using FT-IR, TEM, PSD and magnetic observation. The synthesized Fe3O4 nanoparticles have the characteristic absorption peak of Fe-O bond at 581.96cm-1, and a wide stretch vibration peak of -OH at 3407.84cm-1, with the average hydration particle size of 111.8nm, showing good superparamagnetic properties. Batch adsorption experiments systematically investigated the influence of adsorption time, Fe3O4 nanoparticles using dosage, the initial concentration of Cr(VI), pH value and temperature on Cr(VI) adsorption. The effect of each factor is in order from large to small: pH value, temperature, initial concentration of Cr(VI) and adsorption time. The adsorption kinetic curves were fitted by pseudo-first order and pseudo-second order models. Adsorption data were more consistent with the pseudo-second order kinetic model, with R2 up to 0.9964, indicating a chemical adsorption. The Langmuir and Freundlich adsorption isotherm models were applied to describe equilibrium data. The Langmuir models can better described Cr(VI) adsorption on magnetite nanoparticles, with R2 up to 0.9902. In addition, the effect of ion concentration and type on adsorption was studied, and the results showed that ion strength could not influence adsorption process, Mg2 increased the removal rate significantly, while SO42- reduced the removal rate.
Key Words: wastewater treatment;Fe3O4 magnetic nanoparticles; Cr (VI); adsorption
目 录
第1章 绪论 1
1.1重金属水污染现状 1
1.1.1重金属污水的来源及危害 1
1.1.2含Cr(VI)污水来源及危害 2
1.2重金属污水处理的研究进展 3
1.2.1污水中重金属的检测 3
1.2.2重金属污水处理技术 5
1.2.3含Cr(VI)污水处理研究进展 7
1.3 Fe3O4磁性纳米材料概况 9
1.3.1 Fe3O4的结构与性质 9
1.3.2 Fe3O4的制备 10
1.3.3 Fe3O4在去除污水中重金属Cr(VI)中的应用 11
1.4本课题的主要研究内容及意义 12
第2章 Fe3O4磁珠的制备及表征 14
2.1实验材料 14
2.1.1实验试剂 14
2.1.2实验设备 14
2.2 实验方法 15
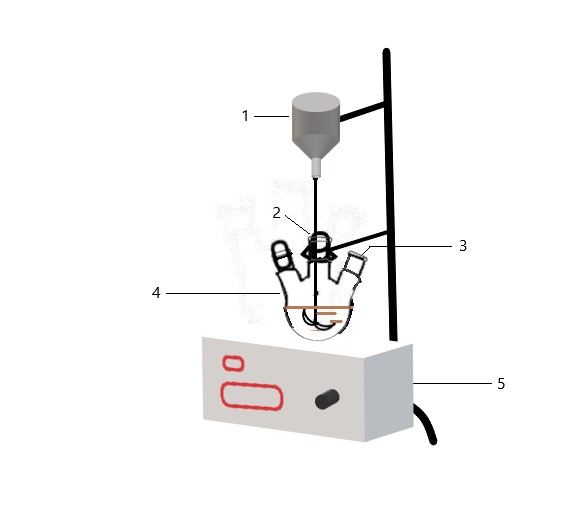
2.2.1 Fe3O4磁珠的制备 15
2.2.2 Fe3O4磁珠的表征 16
2.3结果与讨论 16
2.3.1 FT-IR分析 16
2.3.2 TEM分析 16
2.3.3 PSD分析 18
2.3.4磁性能分析 18
2.4本章小结 19
第3章 Fe3O4磁珠对Cr(VI)的吸附研究 20
3.1实验材料 20
3.1.1实验试剂 20
3.1.2实验设备 20
3.2实验方法 21
3.2.1 Fe3O4磁珠的定量 21
3.2.2 Cr(VI)的标准曲线测定 21
3.2.3 Cr(VI)的吸附试验 22
3.3结果与讨论 24
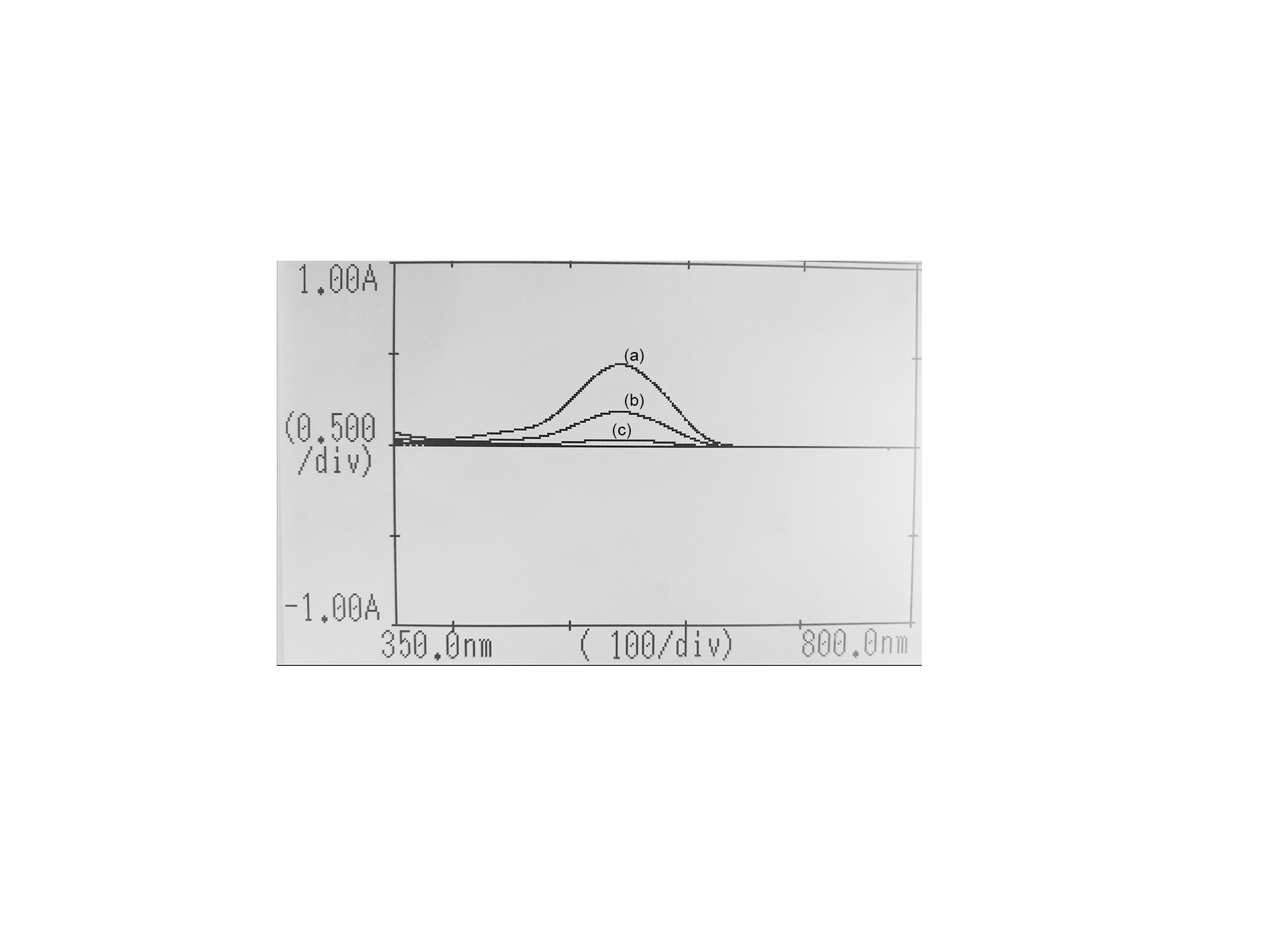
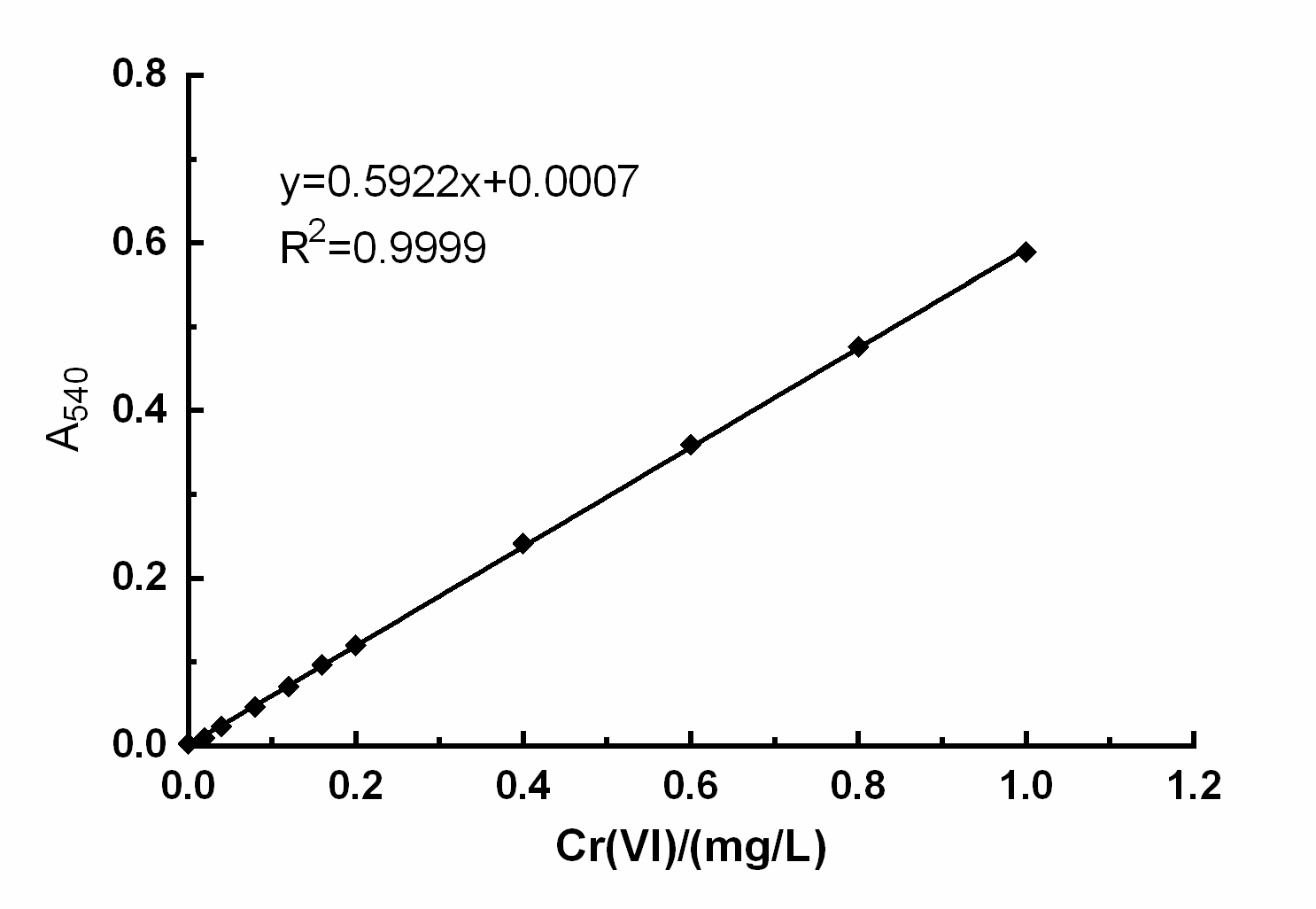
3.3.1 Cr(VI)标准曲线的绘制 24
3.3.2 吸附过程多因素影响分析 25
3.3.3吸附动力学分析 32
3.3.4盐离子对Cr(VI)吸附的作用 35
3.4 本章小结 37
第4章 总结与展望 39
参考文献 40
致谢 45
第1章 绪论
1.1重金属水污染现状
水是不可或缺的生命之源,工业、农业及城市生活用水等模块在不断竞争分配有限的淡水资源,与此同时,宝贵的水资源正面临重金属污染的严重威胁。近年来,科技的迅猛发展大大推进了工业化进程与国家经济建设,但造成的环境问题日益凸显,尤其是由重金属污染,其主要表现为水污染。
自重金属汞造成的“水俣病”等公害病发现以来,重金属污染问题就引起了各国的高度重视,我国于2011年4月初正式批复首个“十二五”专项规划——《重金属污染综合防治“十二五”规划》以防治铬、镉、汞、铅、砷5种重(类)金属。2017年《中国生态环境状况公报》数据表明整体水环境质量正逐步改善,但仍有数据显示部分水体处于重度污染。水利部门流域地下水水质监测井以浅层地下水为主的较差测站和极差测站比例分别为60.9%,14.6%,“三氮”污染较重,个别监测点存在Cr(VI)、Pb、As、Hg等重(类)金属超标现象[1]。近岸海域污水排放总量约为636042万吨,部分直排海污染源排放Hg、Cr(VI)、Pb和Cd等污染物。曾引发多起重金属水污染事件,如广东北江因铜产业造成的铊含量超标变“红水河";国外重金属污水污染状况同样严峻,如美国弗林特铅中毒事件[2],孟加拉国的有28%-62%的人口在饮用被污染的水等[3]。可见,重金属污水的污染状况不容乐观,重金属含量超标不仅会恶化环境质量,也严重危害人体健康,解决该问题迫在眉睫。
1.1.1重金属污水的来源及危害
1.1.1.1重金属污水的来源
重金属污染物的多样性呈指数增长,人为污染源不计其数,主要来源于工业、交通以及生活垃圾,而重金属污水则主要来源于工业废水的排放。矿山开采、金属加工冶炼、氧化电解、电镀、蚀刻、有机颜料、油漆、化工、农药、医药等行业产生的大量污水未经处理直接投放于自然水体,其中的重金属日积月累破坏生态系统,危害公众健康。不同产业产生的重金属种类、形态、含量各异。相关电镀、氧化处理、废旧电池处理、金属加工、蚀刻等行业的污水常含有铬、镉、铜、镍、砷、铅、锌、钒、铂、银和钛元素;印刷电路板制造业中焊接常用到铅、镍元素;木材加工业产生含砷污水;纺织工业、颜料、油漆等行业产生的染色污水含大量铬和镉;胶卷生产中产生大量银等[4]。这些工业生产中产生的污染还可能通过替代品来解决,但矿产开采造成的污染则无法避免,长此以往,后果不堪设想,故如何采取更科学的生产工艺,加大重金属污水处理效率已成为当下的研究焦点。
1.1.1.2重金属污水的危害
重金属在环境污染方面,主要指铬、镉、铅、汞、锌、砷等具有显著生物毒性的元素。一般的天然水体具有自身净化能力,但多个渠道长期排放的重金属早已超过其阈值,改变了水体的性质及组成,此时不能被微生物完全降解的重金属只能通过转化其化学形态或分散以降低毒性,但某些重金属可能转变为毒性更强的物质。未被转化的大量重金属以离子形式存在水溶液中,极易吸附于带负电荷的胶体,随水流迁移,被鱼类、贝类、藻类等生存于被污染的江河湖泊中的水生动物所摄取或渗入土壤污染大量农作物,通过食物链效应由低级生物逐步浓缩至高级生物,最终富集于人体,干扰代谢,引发慢性中毒、癌症甚至死亡,毒性范围一般在1mg/L-10mg/L。砷、铅、镉和汞等重金属已被美国环境保护署以及有毒物质和疾病登记署(ATSDR)列入20大危险物质名单[5]。
重金属污水危害程度取决于重金属种类、含量、理化性质及其存在形式和价态。目前主要关注的元素有锌、铜、镍、汞、铅、镉、砷和铬。其中锌、铜、镍、铬均为人体必需的微量元素。铜参与多种酶与蛋白质的组成、活化,如铜酶参与氧化电子传递链,与铁相互作用催化血红蛋白的合成。过量摄入铜会使蛋白质变性,引起呕吐、抽搐、腹绞痛、溶血、肾功能衰竭和尿毒症等。镍摄入过量可导致心、肺、脑、肾脏退行性病变,接触可致敏导致皮炎[6]。汞、铅、镉和砷均属于人体的非必需元素。汞是一种神经毒素,无机汞通过微生物作用可转化为剧毒的有机汞,如汞的甲基化造成“水俣病”,含量高于0.01mg/L即可导致中毒。铅含量超过2.72µmol/L-3.84µmol/L时可引发中毒,对甲状腺功能、激素分泌、中枢神经系统等造成损伤,引发贫血、失眠、易怒、肌肉无力、幻觉等症状。镉中毒会影响骨钙代谢,使骨节变形、四肢刺痛,发现于日本的“骨痛病”就来源于此。砷大多数以三价亚砷酸盐形式存在于污水中,三价砷可与人体内羟基结合导致慢性中毒,毒性强于五价砷具有“三致”特性[7-9]。
1.1.2含Cr(VI)污水来源及危害
铬(Cr)是一种银白色耐腐蚀的金属,因具有一些特殊的性能广泛应用于工业生产,成为毛皮与制革、轻工纺织、电镀、铬盐及其化合物生产、采矿冶金、有机颜料、染料、油漆、制药等行业的重要原料。这些工业产生的含铬“三废”进入生态循环,对人类健康构成重大威胁。污水中溶解的铬化合物主要以六价和三价形式存在,Cr(VI)毒性比Cr(III)高100倍[10]。轻工纺织、镀铬等行业主要产生Cr(VI)污水,而毛皮与制革、铬盐生产、制药等行业则主要产生Cr(III)污水。因六价铬水溶性强,除工业生产直接排出的污水外,铬渣与粉尘均可通过雨水溶解进入水体,恶化环境。自然水体中铬含量达0.01mg/L便会抑制水体自我净化功能,浓度积累至3mg/L可致死淡水鱼,用含铬污水灌溉农田导致农作物减产,还有一部分铬通过动植物富集累积被人体吸收。因此各国针对铬的排放量制定了严格的标准,例如中国(GB5749-85)生活饮用水水质标准限制六价铬上限为0.05mg/L,中国(GB5048-92)农田灌溉水质标准规定水作、旱作、蔬菜中六价铬含量不超过0.1mg/L,中国(GB11607-89)渔业水质标准限制渔业水域铬含量为0.1mg/L[11-13]。
铬污染的毒性大小主要取决于其价态高低,铬及其化合物的价态有六价、三价、二价以及单质铬,一般随价态增高其毒性增大,二价及单质铬毒性很小或无毒,故目前主要关注Cr(III)和Cr(VI)的危害。铬含量超出临界水平使得水体变黄,逐渐浑浊,且散发异味,生存其中的鱼类易致死,特别的是,Cr(III)对鱼类的毒性要大于Cr(VI)。含铬污水对农作物的毒性也得到验证,尤其对第一季作物危害较大,浓度过高将造成作物萎黄、延缓生长、影响共生固氮作用等,最终使农业减产[14]。与锌、铜类似,铬也是人体必需的微量元素,其中Cr(III)为有益元素,对人体毒害作用小,在人体内参与血糖调节,可保护心血管、控制体重,故主要考虑Cr(VI)对人体的危害。Cr(VI)具有透膜功能,能迅速透过红细胞膜进入细胞,结合血红蛋白,通常经皮肤、消化道和呼吸道侵入人体,引发铬性皮炎、“铬疮”、湿疹,鼻炎、支气管炎、肺硬化、肺癌,反胃呕吐、腹痛、肝肿大甚至死亡[15]。
1.2重金属污水处理的研究进展
1.2.1污水中重金属的检测
污水中重金属离子存在形式不同,含量较低,有效去除重金属的前提是对其进行精准高效的检测,常见的检测方法有原子吸收光谱法、紫外分光光度法、络合滴定法、电化学分析、电感耦合等离子体原子发射光谱法(ICP-AES)、荧光分析法、流动注射分析法以及生物化学分析法等,各方法的对比分析见表1.1[16-18]。国标《GBT5750.6-2006生活饮用水标准检验方法-金属指标》中使用二苯碳酰二肼紫外分光光度法检测水质中六价铬的含量,最低检测质量达0.2μg[19]。Wang[20]等采用氨基苯甲酸作为碳源自制高荧光碳点,通过三价铁与其络合使荧光猝灭的现象检测三价铁含量,检出限为0.05μM。蒋育澄[21]等将流动注射原子吸收法与离子交换吸附柱系统串联实现对三价铬和六价铬的在线富集与形态分析。单一方法检测污水中重金属含量具有较大的局限性,因此采取多种技术联用已成为当前重金属检测的研究热点。
表1.1常见重金属检测技术对比
Table 1.1 Comparison of common heavy metal detection techniques
方法 | 原理 | 优劣势 |
络合滴定法 | 络合反应,络合剂与金属离子形成螯合物而显色 | 快速、稳定,滴定终点明显 干扰因素多,如共存离子、滴定剂、pH、缓冲溶液 |
紫外可见分光光度计法 | 物质本身在190-800nm的吸收波长变化或与显色剂反应 | 简单方便,应用范围广 灵敏度低 |
电化学-阳极溶出法 | 根据元素电化学性质不同作为电化学池的组成部分,通过氧化反应在阳极溶出 | 灵敏度高,快速,成本低,易携带,检测限度低 步骤多,需满足电化学反应条件 |
原子吸收光谱法 | 待测元素的原子蒸汽吸收其特征谱线,使特征谱线强弱程度改变 | 灵敏度高,选择性强,分析范围广,干扰小,精密度高 以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。 相关图片展示:
您需要先支付 80元 才能查看全部内容!立即支付
最新文档

|