芳基磺胺类新型高效H5N1抑制剂的合成及结构活性关系研究外文翻译资料
2022-01-04 22:01:32

英语原文共 11 页,剩余内容已隐藏,支付完成后下载完整资料
欧洲药物化学杂志159 (2018)206e216
内容列表可在ScienceDirect上找到
欧洲药物化学杂志
期刊主页:http: / /www.elsevier .com/locate/ejmech
研究论文
芳基磺胺类新型高效H5N1抑制剂的合成及结构活性关系研究
Yongshi Yu a, Qi Tang b, Zhichao Xu a, Siliang Li b, Mengyu Jin a, Zixuan Zhao b,
Chune Dong a, Shuwen Wu b, *, Hai-Bing Zhou a, **
a .武汉大学药学院,湖北省氟化药物工程技术研究中心,病毒学国家重点实验室,组合生物合成与药物发现教育部重点实验室,武汉430071
b .武汉大学生命科学学院现代病毒学研究中心病毒学国家重点实验室,武汉,430072
a r t i c l e i n f o a b s t r a c t
|
文章历史:2018年7月28日收到2018年9月22日收到修改后的 2018年9月25日接受 2018年9月27日在线提供 |
H5N1病毒是人类感染的高致病性甲型流感病毒的一个亚型,由于其不可预测的高致死率,最近受到了人们的关注。本研究通过系统的结构-活性关系研究,鉴定了一系列芳基磺酰胺衍生物作为改良的H5N1流感病毒抑制剂。其中,最有效的H5N1抑制剂3h对H5N1病毒表现出优异的抗病毒活性,EC50值为0.006 mM,选择性指数为33543.3。此外,3h与M2质子通道蛋白的分子对接为了解该类化合物对H5N1的抑制作用提供了实用途径。copy;2018爱思唯尔马森SAS。保留所有权利。 |
|
关键词:H5N1病毒 高致死率 芳基磺胺类抑制剂 结构-活性关系 |
1. 介绍
流感病毒属于正粘病毒科[1,2],在所有病毒中具有独特的抗原变异性和季节性,对全球健康和经济造成巨大负担。此外,与其他类型(如B型流感和C型流感)相比,A型流感病毒具有更高的抗原突变,可导致各年龄组的发热性呼吸道疾病爆发性暴发,对人类健康构成严重威胁[1e4]。
高致病性禽流感(HPAI) H5N1病毒是一种甲型流感病毒亚型,1997年在香港首次报道[5,6]。根据世界卫生组织(WHO)的最新调查统计,自2003年以来,人类感染H5N1病毒的病例有860例,其中死亡454例,表明H5N1病毒与其他亚型甲型流感病毒相比具有更强的毒性和更高的死亡率[6,7]。由于在流感暴发的初级阶段缺乏有效的H5N1疫苗,因此开发抗病毒药物
*通讯作者。* *通讯作者。
电子邮箱:shuwenwu@hotmail.com (S. Wu), zhouhb@whu.edu.cn (H.-B.)周)。
https://doi.org/10.1016/j.ejmech.2018.09.065
0223 - 5234 /copy;2018爱思唯尔马森SAS。保留所有权利。
流感感染的预防和治疗引起了研究人员的高度关注[8,9]。目前,主要有两类抗流感药物用于对抗流感流行和大流行。金刚烷胺和金刚乙胺是M2质子通道抑制剂,可防止病毒核蛋白(RNPs)[10]脱壳。神经氨酸苷酶(NA)抑制剂(扎那米韦、奥司他韦、帕那米韦和拉尼诺米韦)抑制新形成的病毒颗粒[10]的释放。此外,法维吡拉韦首次被日本批准为针对流感RNA依赖性RNA聚合酶[11]的抗流感药物。然而,耐药H5N1病毒突变体的迅速出现使得迫切需要开发新的抗流感药物[12e18]。因此,努力开发新的抗病毒药物,特别是H5N1抑制剂,对未来控制流感暴发将非常关键。
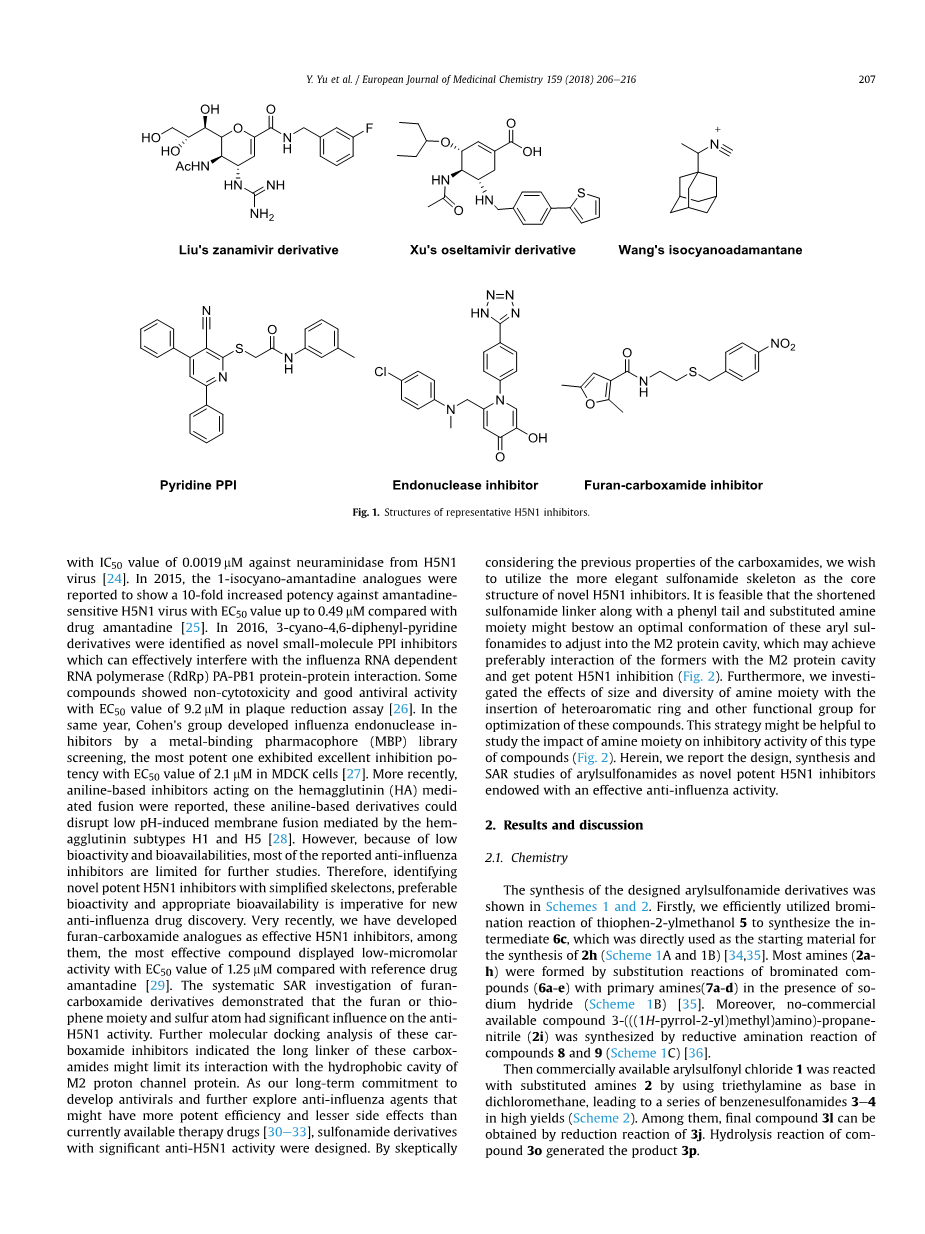
到目前为止,有报道称一些小分子通过对已知的抗流感药物或hit-and-lead发现方法的简单修饰来抑制甲型H5N1流感病毒(图1)[19e22]。2013年,Liu等人开发了修饰的扎那米韦衍生物作为有效的神经氨酸酶抑制剂,IC50值为0.001 mM,测定其对H5N1病毒的抑制活性。这项工作代表了通过知名药物[23]开发改进的抗流感抑制剂的起点。
徐的研究小组发现了一系列奥司他韦衍生物,它们通过靶向150个空腔表现出对n1的强选择性抑制
Y. Yu et al/欧洲药物化学杂志159 (2018)206e216 207
图1所示。典型H5N1抑制剂的结构。
对H5N1病毒[24]神经氨酸酶的IC50值为0.0019 mM。2015年,据报道,1-异氰基金刚烷胺类似物对金刚烷胺敏感的H5N1病毒的效力比药物金刚烷胺[25]提高了10倍,EC50值高达0.49 mM。2016年,3-氰基4,6-二苯基吡啶衍生物被鉴定为新型小分子PPI抑制剂,可有效干扰流感RNA依赖RNA聚合酶(RdRp) PA-PB1蛋白-蛋白相互作用。部分化合物在血小板减少实验[26]中表现出非细胞毒性和良好的抗病毒活性,EC50值为9.2 mM。同年,Cohen团队通过金属结合药效团(MBP)文库筛选,开发出流感内切酶抑制剂,其中最有效的一种在MDCK细胞[27]中表现出极好的抑制作用,EC50值为2.1 mM。近年来,有报道称苯胺类抑制剂作用于血凝素介导的融合,这些苯胺类衍生物可以破坏血凝素亚型H1和H5[28]介导的低ph诱导的膜融合。然而,由于其生物活性和生物利用度较低,目前报道的大多数抗流感抑制剂都受到了进一步研究的限制。因此,寻找具有简化的skelectons、较好的生物活性和适当的生物利用度的新型高效H5N1抑制剂对新的抗流感药物的发现至关重要。最近,我们开发了呋喃-羧酰胺类似物作为有效的H5N1抑制剂,其中最有效的化合物表现出低分子活性,EC50值为1.25 mM,与参考药物金刚烷胺[29]相比。对呋喃-酰胺类化合物进行了系统的合成孔径雷达(SAR)研究,结果表明呋喃或硫离子和硫原子对h5n1的抗h5n1活性有显著影响。进一步的分子对接分析表明,这些car-boxamide抑制剂的长链可能限制其与M2质子通道蛋白疏水腔的相互作用。由于我们长期致力于开发抗病毒药物并进一步探索可能比现有治疗药物更有效和副作用更小的抗流感药物[30e33],因此设计了具有显著抗h5n1活性的磺胺衍生物。由怀疑地
考虑到以往羧基酰胺的特性,我们希望利用更优雅的磺胺骨架作为新型H5N1抑制剂的核心结构。可行,缩短磺酰胺链接器以及苯尾巴和胺代替一部分可能会给一个最优构象的芳基sul-fonamides调整到M2蛋白质腔,这可能达到最好的交互框架与M2蛋白质腔和得到有效的H5N1病毒抑制(图2)。此外,我们研究了胺基的大小和多样性对杂芳环和其他官能团插入的影响,以优化这些化合物。
2. 结果与讨论
2.1。化学
所设计的芳基磺酰胺衍生物的合成如方案1和方案2所示。首先,我们高效利用噻吩-2-酰甲醇5的溴化反应合成中间体6c,该中间体直接作为2h合成的起始材料(方案1A和1B)[34,35]。大多数胺(2a-h)是在so-dium hydride (Scheme 1B)[35]存在下溴化化合物(6a-e)与初生胺(7a-d)取代反应形成的。此外,通过化合物8和9(方案1C)[36]的还原胺化反应,合成了尚未上市的化合物3-(((1H-pyrrol-2-yl)甲基)氨基-丙腈(2i))。
然后将市售的芳基磺酰氯1与取代胺2在二氯甲烷中以三乙胺为基础反应,得到一系列高收率的苯磺胺类3e4(方案2),其中最终化合物3l通过3j还原反应得到。化合物3o水解反应生成产物3p。
Y. Yu et al/欧洲药物化学杂志159 (2018)206e216 208
图2所示。设计新型H5N1抑制剂的策略。
方案1。胺中间体2a-i的合成。(a) PBr3 (0.1eq)、Et2O、0 C、1 h;(b) NaH (1.2eq)、DMF、rt、16 h;(c) NaBH4 (0.5eq), MeOH, rt, 6h, 3h。
方案2。芳基磺酰胺衍生物3-4的合成。(a) Et3N (1.2 eq)、DCM、rt、8e12 h;(b) Fe (5 eq), NH4Cl (10 eq), MeOH/H2O (4:1), 60 C, 6 h;(c) NaOH(15%)、EtOH、rt、过夜。
2.2。结构与活性关系研究
所有获得的新型芳基磺酰胺衍生物均通过MDCK细胞的血小板减少试验(PRA)检测其对H5N1病毒的抑制作用。为了消除细胞毒性作用对h5n1抗体活性的影响,我们还用MTT法检测了芳基磺胺类似物在MDCK细胞中的细胞毒性。此外,对抗流感药物金刚烷胺进行了对照试验。生物活性结果如表1所示,并对这些化合物的结构-活性关系(SAR)进行了研究。
在全球观察,所有合成化合物3 - z和4 a - b显示抗H5N1病毒的抑制效力之间的介质微摩尔的范围(EC50frac14;47.59毫米)摩尔范围(EC50frac14;0.006毫米)。其中,4-cyano-N——(2-cyanoethyl) - n - (thiophen-2-ylmethyl) benzenesulfonamide 3 h是最强有力的H5N1病毒抑制剂(EC50frac14;0.006毫米,如果gt; 33543.5)和显示
更高的EC50值与金刚烷胺(表1,进入8)。最初,设计磺酰胺化合物3 j显示良好的抗病毒活性对H5N1病毒(EC50frac14;3.56毫米)(表1,进入10)。通过改变R1、R2、R3取代基进一步修饰3j,研究了取代基的位置和性质对抑制活性的影响。首先,我们合成芳基磺酰胺衍生物(3a-3c,表1,分项1e3),苯环上分别有o-F、m-F和p-F取代基。抗h5n1活性结果显示,meta-和对取代苯基类似物(3b和3c,表1,条目2e3)比正取代类似物3a(表1,条目1)更有效。为了进一步研究这一先导,我们还制备了同源呋喃类似物进行比较。我们发现,与元取代的类似物3x相比,副取代的类似物3t显示出8倍的效力(表1,条目20 vs 24)。这些结果表明苯环上的对取代基R1对抑制活性最有利
Y. Yu et al/欧洲药物化学杂志159 (2018)206e216 209
表1
芳基磺酰胺类似物对H5N1病毒的抗流感评价。
|
条目 |
化合物 |
EC50(毫米) |
CC50 (mM) b |
原文如此 |
|
1、2、3、5、6、7、8、10、11、13、14、15、17、18、19、21、22、23、24、26、26、27、28、29 |
3a 3b 3c 3d 3e 3f 3g 3h 3i 3j 3k 3l 3m 3n 3o 3p 3q 3r 3s 3t 3u 3v 3w 3x 3y 3z 4a 4b金刚烷胺 |
0.95plusmn;0.22 - 0.099plusmn;0.03 0.099plusmn;0.02 - 0.48plusmn;0.099 - 0.02plusmn;0.09 0.33plusmn;0.08 - 2.25plusmn;0.33 - 0.08plusmn;0.003 1.77plusmn;0.50 - 3.56plusmn;1.77 - 0.50plusmn;3.66 2.37plusmn;0.80 - 1.33plusmn;2.37 - 0.80plusmn;0.06 1.54plusmn;0.49 - 47.59plusmn;1.54 - 0.49plusmn;0.09 0.50plusmn;0.19 - 4.25plusmn;0.50 - 0.19plusmn;0.14 8.33plusmn;3.19 - 0.20plusmn;8.33 - 3.19plusmn;8.22 4.23plusmn;1.21 - 3.20plusmn;4.23 - 1.21plusmn;0.13 0.64plusmn;0.12 - 8.05plusmn;0.64 - 0.12plusmn;0.06 |
gt; 205.62 gt; 205.62 gt; 205.62 gt; 195.69 gt; 173.11 126.71plusmn;38.39 gt; 198.26 gt; 201.26 gt; 178.15 gt; 189.81 gt; 191.42 gt; 207.52 - 81.00plusmn;18.91 gt; 178.19 gt; 154.27 gt; 164.98 gt; 216.32 gt; 205.37 gt; 180.65 gt; 219.15 gt; 208.20 gt; 211.51 gt; 186.14 gt; 219.15 gt; 226.64 gt; 209.50 gt; 181.13 - 115.63plusmn;28.68 gt; 440.99 |
gt;216.4 bgt; 2076.9 gt;2076.9 gt;407.7 gt; 58.1 gt;33543.3 gt;100.6 gt;53.3 gt;1 891.0 gt;5 3.5 gt;4 584.6 gt;5 42.5 gt;7 25.0 gt;9 1057.6 gt;0 8.5 gt;1 51.8 gt;4 283.0 14.4 gt;5 1917.3 |
|
一个 a EC50:有效抑制50%病毒斑块形成的浓度。 全文共30415字,剩余内容已隐藏,支付完成后下载完整资料 资料编号:[2275] |
||||




