Cu2OTiO2光催化材料的制备及其光催化性能的研究毕业论文
2020-04-07 14:06:51
摘 要
光催化技术在解决环境污染问题中的应用越来越受到各界的关注。二氧化钛(TiO2)由于其具有地球丰富度、环境友好性、安全性和化学稳定性等性质,在许多领域得到了广泛的研究。其在降解和制氢方面表现出了优异的性能,但是TiO2具有宽带隙(约3.2 eV)、电子/空穴容易复合的缺点,导致量子产率偏低且对光的吸收有很大的局限性,限制了它的发展。
为了扩展TiO2的光响应范围,可以采取表面修饰的方法改善其对太阳光的吸收。并且提高TiO2半导体光催化剂降解性能的作用。助剂修饰是近几年广泛应用的一种方法来拓展TiO2的吸收光范围,本文旨在通过将Cu2O作为助剂修饰TiO2半导体结合来合成Cu2O/TiO2。通过抑制了电子和空穴的复合,达到延长了电子和空穴的寿命的目的,从而提高了光催化剂的催化活性。
本文是以Cu(NO3)2和三聚氰胺为前驱体原料,合成Cu-三聚氰胺纳米管前驱体。并以该管状结构为模板,合成二氧化钛。本实验条件是在550oC下煅烧形成Cu2O/TiO2纳米复合材料。实验结果表明,当Cu2O含量为1 wt%时,光催化降解性能最好。因为在光照下,激发到TiO2导带的电子将转移到Cu2O,Cu2O把电子进一步转移出去,从而减少了电子/空穴的复合,提高降解污染物的性能。
本文的特点是:不同于传统的制备Cu2O/TiO2方法,本文以Cu-三聚氰胺纳米管为前驱体进行TiO2改性。在本实验中,以Cu-三聚氰胺纳米线为前驱体制备了Cu2O/TiO2复合材料,为TiO2的改性提供了一种新方法。
关键词:Cu2O/TiO2;光催化降解;助剂修饰。
Abstract
The application of photocatalytic technology in solving environmental pollution problems has attracted more and more attention from all walks of life. Titanium dioxide (TiO2) has been extensively studied in many fields because of its richness, environmental friendliness, safety, and chemical stability. It exhibits excellent performance in terms of degradation and hydrogen production, but TiO2 has a wide bandgap (about 3.2 eV) and electron/hole recombination is easily disadvantageous, resulting in low quantum yield and very high light absorption. The big limitations have limited its development.
In order to expand the photoresponse range of TiO2, surface modification can be used to improve its absorption of sunlight. And improve the role of TiO2 semiconductor photocatalyst degradation performance. The auxiliary modification is widely used in recent years to expand the absorption range of TiO2. This paper aims to synthesize Cu2O/TiO2 by using Cu2O as a cocatalyst to modify TiO2 semiconductors. By suppressing the recombination of electrons and holes, the purpose of prolonging the life of electrons and holes is achieved, thereby improving the catalytic activity of the photocatalyst.
In this paper, the precursor of Cu-melamine nanotubes was synthesized using Cu(NO3)2 and melamine as raw materials. Using this tubular structure as a template, titanium dioxide was synthesized. The experimental conditions were calcination at 550oC to form Cu2O/TiO2 nanocomposites. When Cu2O content is 1 wt%, the photocatalytic degradation performance is best. Because in the light, the excited electrons on the TiO2 are transferred to Cu2O, and Cu2O transfers further electrons. This reduces the recombination of electrons and holes and improves the performance of degrading contaminants.
The innovation of this paper is that different compared with traditional preparation of the Cu2O/TiO2 method, Cu2O/TiO2 is prepared by Cu source as a precursor. In this experiment, Cu2O/TiO2 composites were prepared using Cu-melamine nanowires as precursors, which can provide a new method for the modification of TiO2.
Key Words:Cu2O/TiO2;photocatalytic degradation;cocatalyst modification.
II
目 录
第1章 绪论 1
1.1 研究背景及发展 1
1.2 光催化降解机理 1
1.3 TiO2半导体光催化 2
1.3.1 TiO2的光催化原理 2
1.3.2 TiO2的制备方式 3
1.4 提高光催化材料性能的改性方法 4
1.4.1 贵金属的沉积 4
1.4.2 离子的掺杂 4
1.4.3 半导体的复合 5
1.4.4 表面敏化 5
1.5助剂修饰TiO2光催化降解研究进展 6
1.6 本论文的研究意义与主要内容 6
第2章 实验部分 8
2.1 实验试剂和仪器 8
2.1.1 实验试剂 8
2.1.2 实验仪器 8
2.2 实验样品的制备 9
2.2.1 Cu-三聚氰胺纳米线的制备 9
2.2.2 Cu2O/TiO2光催化材料的制备 9
2.3 样品测试与表征 9
2.4 样品光催化性能测试 10
第3章 结果与讨论 11
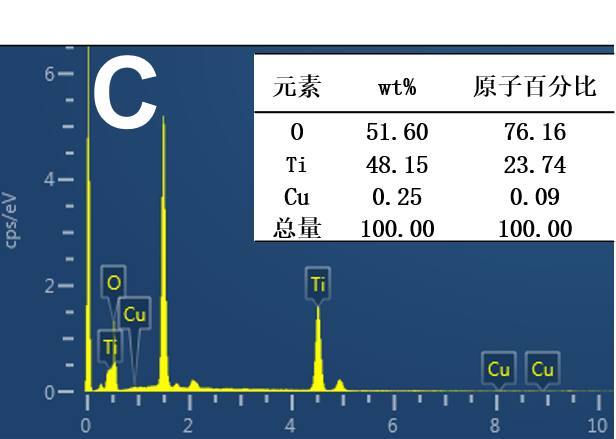
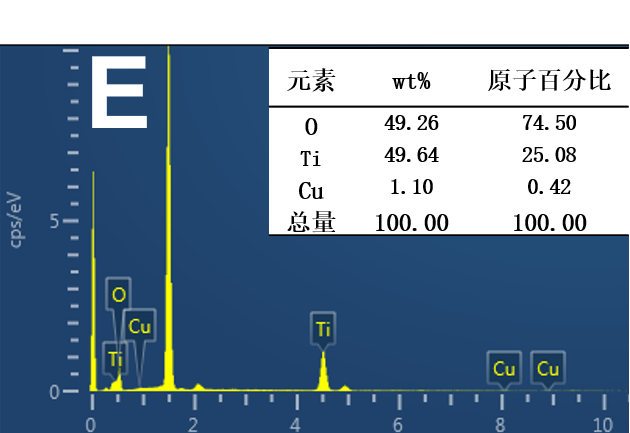
3.1 样品表征结果 11
3.1.1 样品的XRD表征结果 11
3.1.2 样品的FESEM表征结果 12
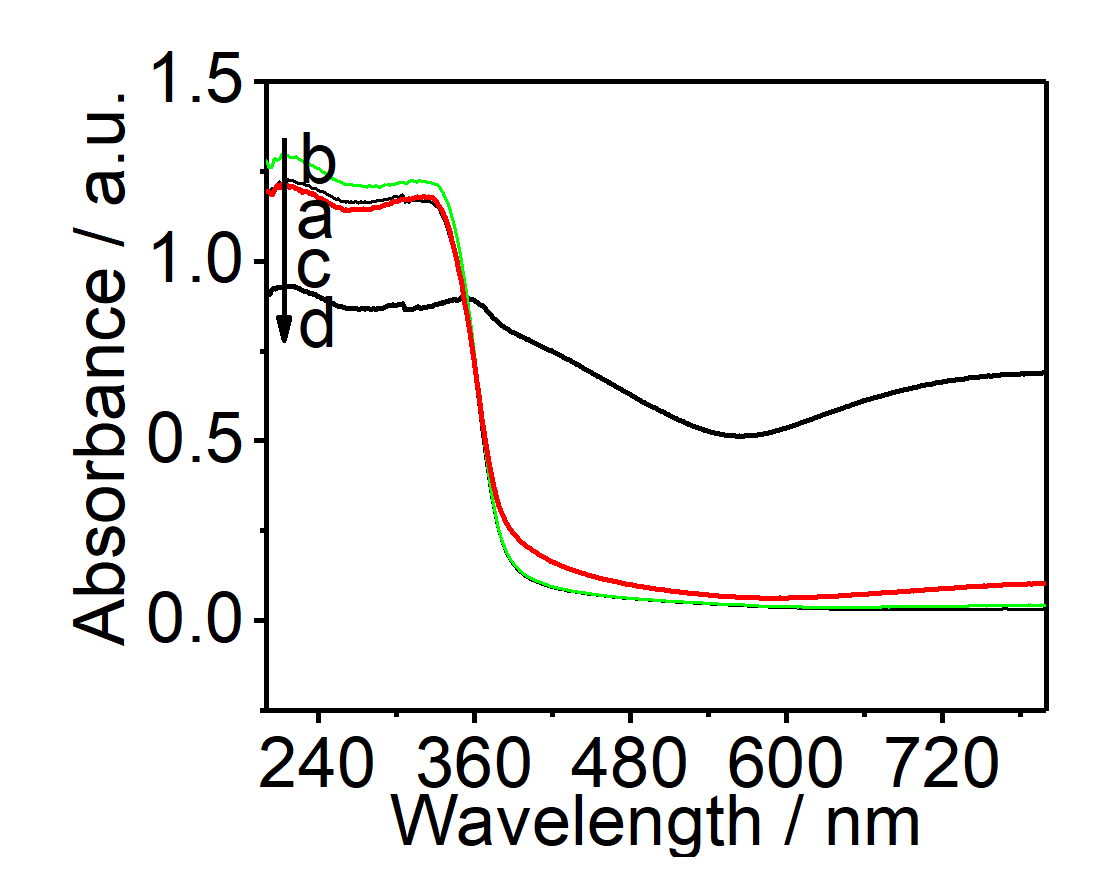
3.1.3 样品的UV-vis表征结果 13
3.2 光催化降解性能及降解机理 13
3.2.1 样品的光催化降解性能 13
3.1.2 样品的光催化降解机理 14
第4章 结论与展望 15
4.1 结论 15
4.2 展望 15
参考文献 16
致谢 19
第1章 绪论
1.1 研究背景及发展
当今情况下,随着社会和经济快速发展,能源短缺和环境污染已经成为人类所面临的重要问题。因此现阶段的研究工作者大都致力于解决能源短缺与环境污染这两大问题,这就迫切要求开发出高效、低能耗、应用范围广、环境污染少的功能材料,以实现可持续发展。随着工业的迅猛发展,经济发展的同时也带来了环境污染。由于水与人类的生存密不可分,因此研究最多的也就是水的处理方法。染料产业发展在工业发展中最为迅猛,而其中最主要的就是染料生产中的废水排放,由于废水具有成分比较复杂、色泽较深、大多为酸性等特点[1],故而无法简单的进行处理。常见的废水处理方法有物化法[2]、生化法[3]和化学法[4]。近年来,由于印染行业的发展需要,具有抗氧化、抗光解的染料被研究出来。这大大加大了废水的处理难度。单一的废水处理方式已经无法处理这些废水,于是组合技术应运而生。像将物化法和生化法组合技术[5]、光催化氧化与生物氧化组合技术[6]等组合处理技术已经运用于实践之中。这些技术将各自的优势展现的同时又相互补充,能够更大效率的处理废水,较单一废水处理方式有了极大进步。但由于物化法主要以吸附为前提,操作较繁琐且成本较高;生化法对于废水的酸碱度、藻类以及水中生物存在要求较高;化学法具有成本高、毒性大等缺点。故而在联合各项技术的同时应该寻找更加易于操作且较为实惠的方法。自研究[7]表明半导体二氧化钛具有分解水的功能后,二氧化钛被广泛研究。因TiO2具有活性高、热稳定性高、抗氧化性强、价格便宜等基础特点。且现如今TiO2越来越多的优异性能像降解和制氢等被发掘出来,使得TiO2的运用也越来越广泛。例如有序的介孔黑色TiO2(OMBT)材料具有更大的比表面积和孔径,更重要的是其能够将介孔原本的紫外吸收扩展到可见光和红外区域[8]。除此之外,TiO2作为NO2、CO传感器的应用[9]也被报道了出来。随着不断地研究发现,单纯的TiO2已经无法满足发展的需要。于是关于如何对TiO2进行改性,使其具有更优异的性能成为现如今研究TiO2的重点。
1.2 光催化降解机理
光催化技术是指以光能为能量来源,降解有机污染物、光催化分解水、还原重金属离子等。是一种绿色、无污染的环境处理技术。半导体光催化剂在可见光照射下,产生光生电子和光生电子空穴。导带电子具有还原性,一般与其表面吸附的氧分子与之进行一系列的反应可以生成·OH、·O2-、HO2·、H2O2等来降解有机物。空穴能吸收半导体表面的电子,直接与之反应。而光生空穴具有强氧化性,可以与催化表面吸附的H2O和OH-反应生成·OH来降解氧化物。这就使得其表面的物质可以被氧化分解掉[10]。从理论上讲,半导体有可能作为光催化剂的必要条件是:当半导体吸收的光能不小于其带隙能,足以激发半导体产生电子和空穴。图1.1显示了半导体光催化降解水的原理图。
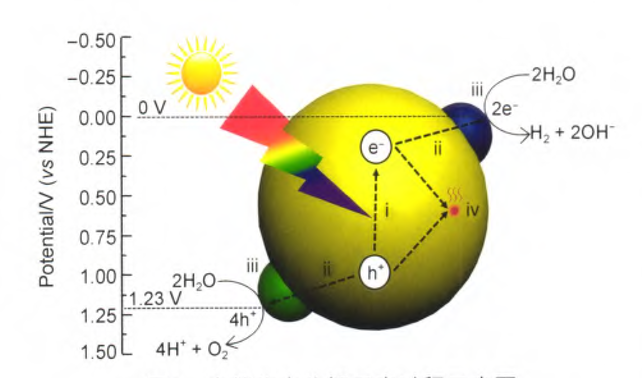
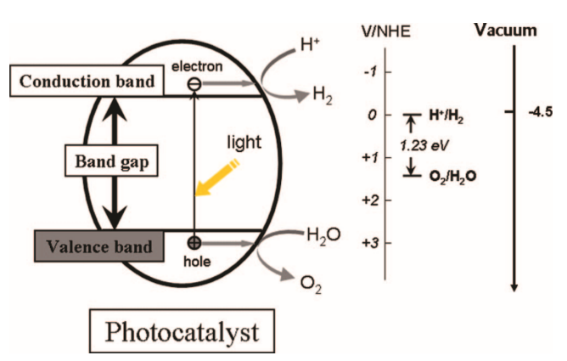
图 1.1 半导体光催化降解原理图[11]
(i)光电子/空穴对的产生:在太阳光照射下,若照射能量大于半导体禁带宽度(hνgt;Eg),半导体催化材料价带上的电子被激发跃迁到导带上。经过该过程,导带上产生了带负电的高活性电子(eCB-),价带上则留下带正电荷(hνB )的空穴。电子/空穴对由此形成;(ii)电子和空穴的迁移:光电载流子和空穴分别迁移到半导体材料的表面;(iii)表面反应:迁移到表面的光生电子参与水的还原反应,将水还原成氢气。空穴则参与水的氧化反应,将水氧化生成氧气。总的反应方程式为H2O→l/2O2 H2。(iv)电子和空穴的复合损失:被激发的电子/空穴对重新相遇时会发生复合,这种相遇可能在材料内部和表面附近。复合的结果是以热和光辐射的形式释放能量。结合半导体催化的原理和热力学可以知道,当半导体的导带和价带位置与水的还原和氧化电位相匹配(即半导体导带底的能级必须比水的还原产氢电位更负),同时其价带顶的能级比水的氧化产氧电位更正时,激发的电子/空穴对才有足够的能力进行水的还原和氧化反应。当电子和空穴发生复合时,会使得光催化降解效率降低,因此寻找合适的方法使得电子/空穴之间的复合时间减短是一种增加光催化效果的方法。
1.3 TiO2半导体光催化
1.3.1 TiO2的光催化原理
自从上世纪70年代Fujishima发现TiO2在紫外光的照射下可以分解水[7]以来,TiO2半导体光催化逐渐走入了人们的视野。现如今新型的TiO2广泛应用于传感器[12]和染料敏化太阳能电池[13]等方面。纳米TiO2是一种n型半导体材料,也是一种无机金属氧化物。TiO2具有锐钛矿、金红石和板钛矿三种晶型,它们的禁带宽度[14]分别为3.2 eV、2.96 eV、3.02 eV。所谓的禁带是指半导体材料存在的导带与价带之间的区域,它与半导体能否具有光催化作用有着密切的联系。当光照能量不小于禁带宽度时,半导体价带上的电子被激发,与此同时,价带上会产生空穴。而电子/空穴的产生可以使得其具有光催化作用。
半导体TiO2能进行光催化是由于TiO2的带隙能一般为-0.2~3.0 eV,理论上讲,只要半导体吸收的光能不小于TiO2带隙能时,TiO2价带上的电子被激发迁移至导带,即可形成电子/空穴对。图1.2为TiO2光催化示意图:
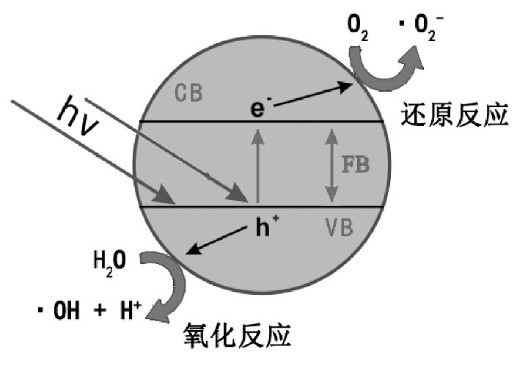
图 1.2 TiO2光催化示意图
光催化基于光电化学的反应,涉及由于光照的影响而生成的电子和空穴。可以将光催化过程用下面的化学式来进行简单的分析:
hν→eCB- hVB
H2O h VB→OH· H
O2 e-CB→·O2-
且该光催化反应在偏碱性溶液中,还原反应会更难一些。一方面是因为大气中CO2的存在且其具有酸性可以吸收可缓冲溶液的pH,另一方面是因为在碱性溶液中更容易发生O2还原。TiO2的禁带宽度为3.2 eV,在紫外光区具有较好的光催化作用。但TiO2的导带对高活性电子的捕获能力有限,容易导致高活性电子和空穴的再复合。电子和空穴的复合会降低光催化效率,且TiO2光吸收仅限制于紫外区。这导致TiO2对可见光的吸收较为欠缺,为了解决该问题则需要对TiO2进行改性以达到更好的光催化效果。
1.3.2 TiO2的制备方式
目前,制备TiO2常用的原料有:TiCl4、Ti(OR)4、TiOSO4、Ti(SO4)2、Ti、TiO2等。而利用这些原料合成TiO2的常见方式有水热法、溶胶-凝胶法和沉积法。Yu等[15]通过在氟掺杂二氧化锡(FTO)导电玻璃反应釜中添加适量的钛酸丁酯、氯化钠和盐酸,利用水热法在150oC下反应12h,制备出了双层的TiO2结构。施国栋等[16]以Ti(SO4)2为原料,利用氟硅酸控制其结构,在Ti4 、F-、 H2O的摩尔比为1:4.5:15时水热结晶,制得TiO2微球。该TiO2微球在降解亚甲基橙方面具有很好的效果,降解的速率常数可以达到0.023。且这种水热法的成本较为低廉,在未来有望大量生产。用溶胶-凝胶法制备纳米TiO2常用的原料是无机钛盐,如钛酸丁酯Ti(OR)4、 Ti(SO4)2、TiCl4等;Cassaignon等[17]在搅拌条件下将TiCl3的盐酸溶液加入到过量去离子水中,回流处理后得到了三种晶型(金红石、锐钛矿、板钛矿)混合的纳米TiO2粉末。廖东亮等[18]研究了不同抑制剂及凝胶时间对而二氧化钛性能的影响。他们以钛酸丁酯Ti(OR)4为原料,用溶胶-凝胶法制备二氧化钛粉末和纳米二氧化钛薄膜。结果表明,若是简单制备二氧化钛,只需要以冰醋酸为抑制剂,凝胶时间5~10 h即可。但若是需要制备出纳米二氧化钛薄膜,则需要以乙酰丙酮为抑制剂,将凝胶时间应控制在48~72 h。Hirotsugu Nagayama等[19]首次将液相沉积法这一新型纳米制备技术提出来,该方法是在金属氟化物的水溶液中将金属氧化物沉积在基片上,从而制得TiO2的一种方法。周磊等[20]人在此基础上研究了热处理对TiO2光催化的影响。他们在(NH4)2TiF6水溶液中加入H3BO3的水溶液和少量的锐钛矿纳米晶,沉积后得到的TiO2薄膜。该TiO2薄膜在350oC下热处理后光催化活性为未热处理的5倍。
1.4 提高光催化材料性能的改性方法
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: