界面活性位点修饰AuTiO2增强其光催化制氢性能的研究毕业论文
2020-04-07 14:06:30
摘 要
基于半导体设计的光解水制氢被视为解决能源问题的最佳方式之一。TiO2由于良好的化学稳定、无毒、较高的催化活性、成本较低等优点被视为最具有潜力的光催化剂之一。然而,TiO2对可见光利用率较低、空穴电子对极易复合等缺点限制了TiO2在光催化领域的进一步发展。为了进一步增强其光催化性能,需要对TiO2进行改性。
近些年来,贵金属沉积提高光催化制氢性能由于其操作简单而得到广泛应用。传统Pt既能很好地传输电子,表面又有大量活性位点,因而成为报道最多的贵金属助剂。但其成本高昂,实际应用难以实现。贵金属Au也是很好的传输电子体,但是由于其表面缺少活性位点,导致了Au沉积的半导体制氢性能有限。因此,对于缺少活性位点的Au表面修饰活性位点显得十分重要。本文通过传统光沉积法和简单浸渍法成功制备了(NH2)2CS-Au/TiO2光催化剂,测定了其光催化制氢性能。
本论文的研究内容如下:(NH2)2CS-Au/TiO2光催化剂的制备采用两步法。第一步以传统光沉积法制备Au/TiO2,第二步以简单浸渍法使Au选择性吸附(NH2)2CS制备(NH2)2CS-Au/TiO2光催化剂。探索了不同浓度的(NH2)2CS对Au/TiO2制氢性能的影响,并确定了最优方案,测定光催化剂的稳定性。研究结果表明:当(NH2)2CS的浓度为0.05 mmol/L时,(NH2)2CS-Au/TiO2(0.05 mM)光催化制氢速率达到最高为120.15 μmol h−1,分别是Au/TiO2和纯TiO2的1.59倍和47.49倍。Au选择性吸附(NH2)2CS提升光催化制氢性能的原理是:Au作为电子助剂以快速捕获和传输电子,(NH2)2CS作为界面活性位点可以捕获H ,促进H2的还原反应,两种助剂协同提高TiO2光催化制氢性能。
本论文的特色:以表面修饰结合贵金属沉积对TiO2进行改性,显著提高光催化制氢性能,为其他光催化剂改性提供了一种新的思路。
关键词:TiO2;光催化制氢;Au;界面活性位点;硫脲
Abstract
Photocatalytic H2-evolution from water splitting based on semiconductor has been regarded as one of the most potential solutions to resolve the serious energy crisis. Among various semiconductor photocatalysts, TiO2 is one of the most well-known and excellent photocatalytic materials due to its excellent chemical properties, good stability, and non-toxic harmless. However, the pure TiO2 usually exhibits a limited photocatalytic activity owing to the rapid recombination of photogenerated electrons and holes in the bulk or on its surface . To improve the photocatalytic performance of TiO2, various strategies have been widely developed such as semiconductor coupling.
For noble metal cocatalyst-modified photocatalysts with a high H2-evolution performance, both of the rapid electron transfer (or electron capture) from semiconductor to cocatalyst and the following interfacial catalysis for H2 production on the cocatalyst surface are highly required. Compared with Pt-loaded photocatalyst, Au modified sample usually shows an obviously lower H2-evolution activity due to its inefficient H2-production rate on the Au cocatalyst surface. In this paper, The (NH2)2CS-Au/TiO2 photocatalysts were synthesized via a two-step process including the initial photoinduced deposition of Au nanoparticles on TiO2 surface and the following selective adsorption of (NH2)2CS on the Au surface by an impregnation method. Photocatalytic experimental results indicated that all resulted (NH2)2CS-Au/TiO2 photocatalysts exhibited obvously high H2-production performance. The highest H2-production rate of the resultant (NH2)2CS-Au/TiO2(0.05 mM) reached 120.15 μmol h-1, while this value was higher than that of the pure TiO2 and Au/TiO2 by a factor of 47.59 and 1.59, respectively. The enhanced H2-evolution performance of (NH2)2CS-Au/TiO2 can be attributed to the excellent synergistic effect of Au and (NH2)2CS, namely, the Au nanoparticle functions as an effective electrontransfer mediator for the steady capture and rapid transportation of photogenerated electrons from TiO2 surface, while the adsorbed (NH2)2CS serves as the interfacial catalytic active-site to effectively adsorb H ions from solution and promote the rapid H2-evolution reaction.
The innovation of this paper:The present synergistic mechanism of electron-transfer mediator and interfacial catalytic active-sites may provide some new insights for the design of highly efficient photocatalytic materials.
Key Words:TiO2;photocatalytic hydrogen production;Au;interfacial active-sites;sulfourea
目 录
摘 要 I
Abstract II
第1章 绪论 1
1.1 研究背景及发展 1
1.2 TiO2光催化制氢机理 1
1.3提高TiO2光催化制氢的方法 2
1.3.1 元素掺杂 2
1.3.2 半导体复合 3
1.3.3 染料敏化 4
1.3.4 贵金属沉积 4
1.4 贵金属修饰TiO2光催化制氢研究进展 5
1.5 本论文的研究意义与主要内容 5
第2章 实验部分 7
2.1 实验试剂和仪器 7
2.1.1 实验试剂 7
2.1.2实验仪器 7
2.2 实验样品的制备 7
2.2.1 TiO2光催化剂的制备 7
2.2.2 Au/TiO2光催化剂的制备 7
2.2.3硫脲修饰Au/TiO2光催化剂的制备 8
2.3样品的表征手段 8
2.4 样品的光催化制氢性能测试 8
2.5 样品的电化学测试 9
第3章 结果与讨论 10
3.1 样品的表征结果 10
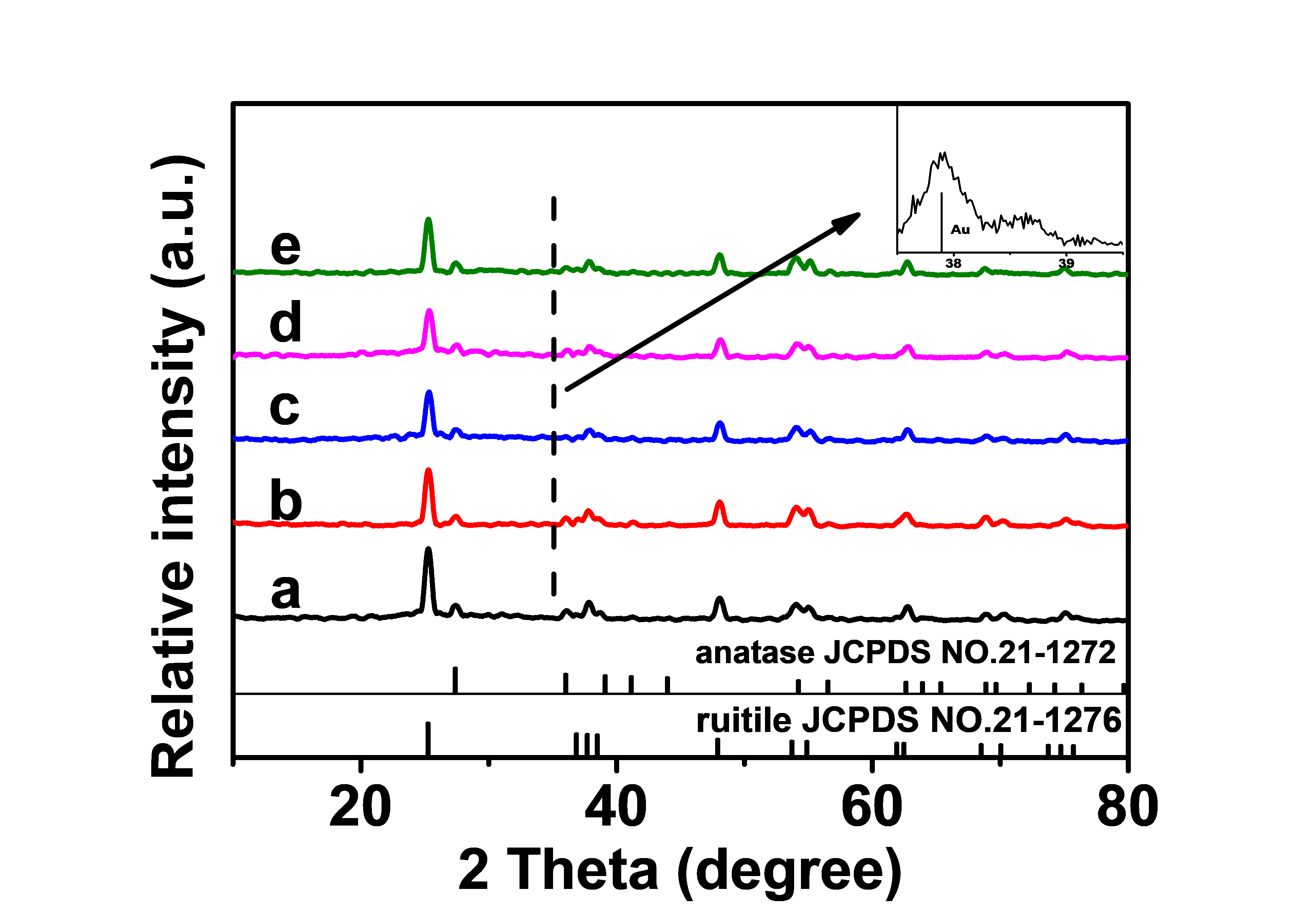
3.1.1 样品的XRD表征结果 10
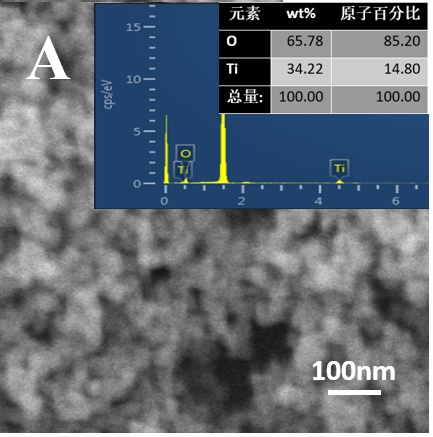
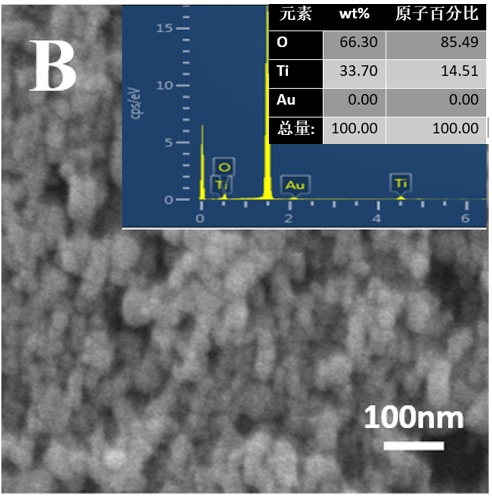
3.1.2 样品的FESEM表征结果 10
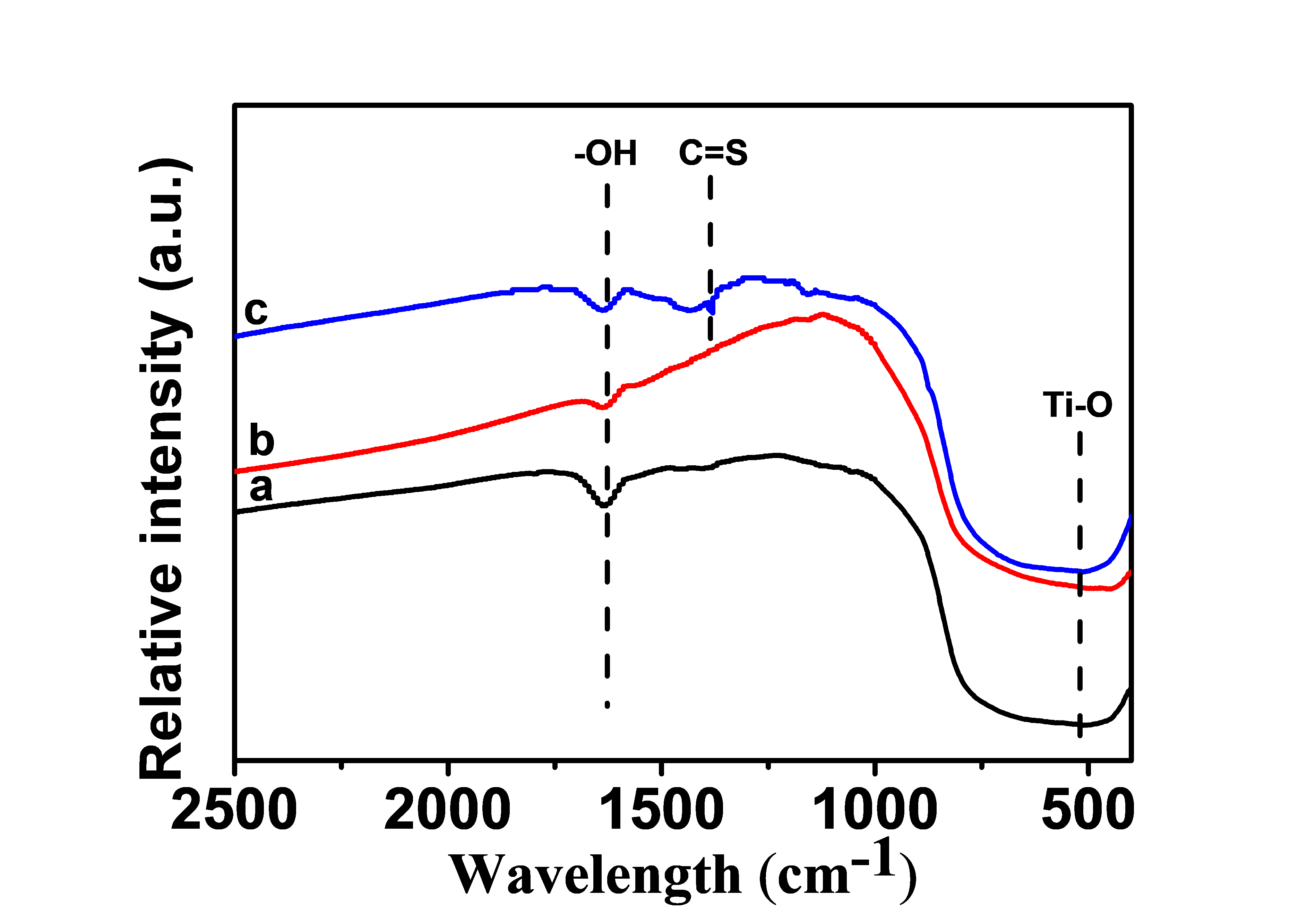
3.1.3 样品的红外表征结果 11
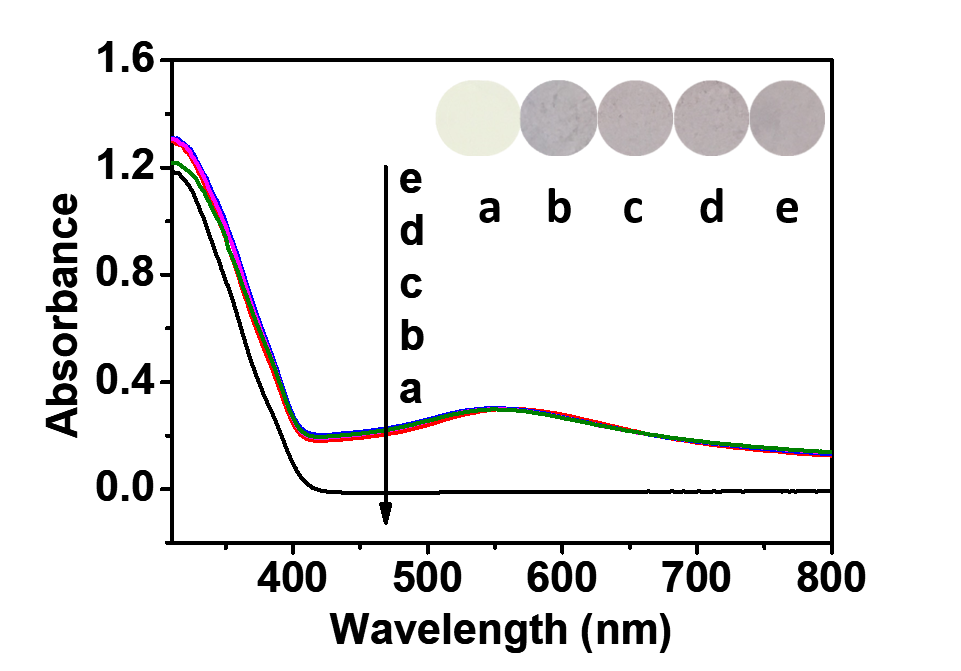
3.1.4 样品的UV-vis表征结果 12
3.2 制氢性能及制氢机理 13
3.2.1 制氢性能 13
3.2.2 制氢机理 14
3.2.3 样品的光电流表征结果 15
第4章 结论与展望 17
4.1 结论 17
4.2 展望 17
参考文献 18
致 谢 21
本科期间参加的科研项目和发表的论文相关 22
第1章 绪论
1.1 研究背景及发展
在人类社会与经济科技发展不断实现新跨越的同时,人类对于能源的需求逐渐增大。然而化石能源的过度开发和使用,煤炭、天然气、石油等不可再生能源却在日益减少,因此产生的生态环境问题也严重影响了人们的生活。据统计,目前全球的的石油储量仅够在使用41年,可再生的清洁能源的发展已经成为全人类共同关心的重大课题。氢气作为能源不仅具有可再生、清洁、产物无污染等优点,并且相比于传统化石燃料,如,天然气(4.5×104 kJ/kg),具有更高的燃烧热(14.19×104 kJ/kg)[1]。因而,氢能的制备和利用可望解决能源问题。
制氢的传统方式有电解水制氢和水煤气法制氢[2],这些方法依然需要利用不可再生能源,不能从根本上解决问题。作为一项新兴的但正在不断成熟的技术,光催化制氢由于其使利用取之不尽的太阳能,且不产生二次污染的优点,引起人们广泛的关注。
1972年,两位日本东京大学的教授Fujishima A和Honda K[3]第一次报告TiO2半导体能够光催化分解水从而产生氢气,拉开了利用太阳能直接分解水制氢的研究序幕,也引发了研究者们对于有关半导体光催化制氢研究的热潮。在现今发现可以作为光催化剂的半导体材料中,TiO2由于具有较高的化学稳定性,带隙宽,无毒无污染,抗光腐蚀等优点,被认为是光催化研究领域中经典的氧化物材料[4]。
1.2 TiO2光催化制氢机理
半导体的电子结构在半导体光催化中起着关键的作用,半导体能带结构由价带(VB)和导带(CB)组成,两个能级之间的能量差称为带隙(Eg)。当半导体受到高于或等于其带隙的光子辐射时,电子吸收光子能量被激发到导带成为光生电子(e-),同时在价带上产生空穴(h )。对于TiO2半导体,反应表示为[5]:
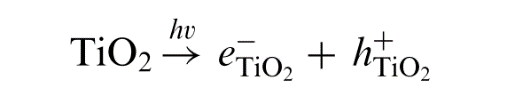 (1.1)
(1.1)
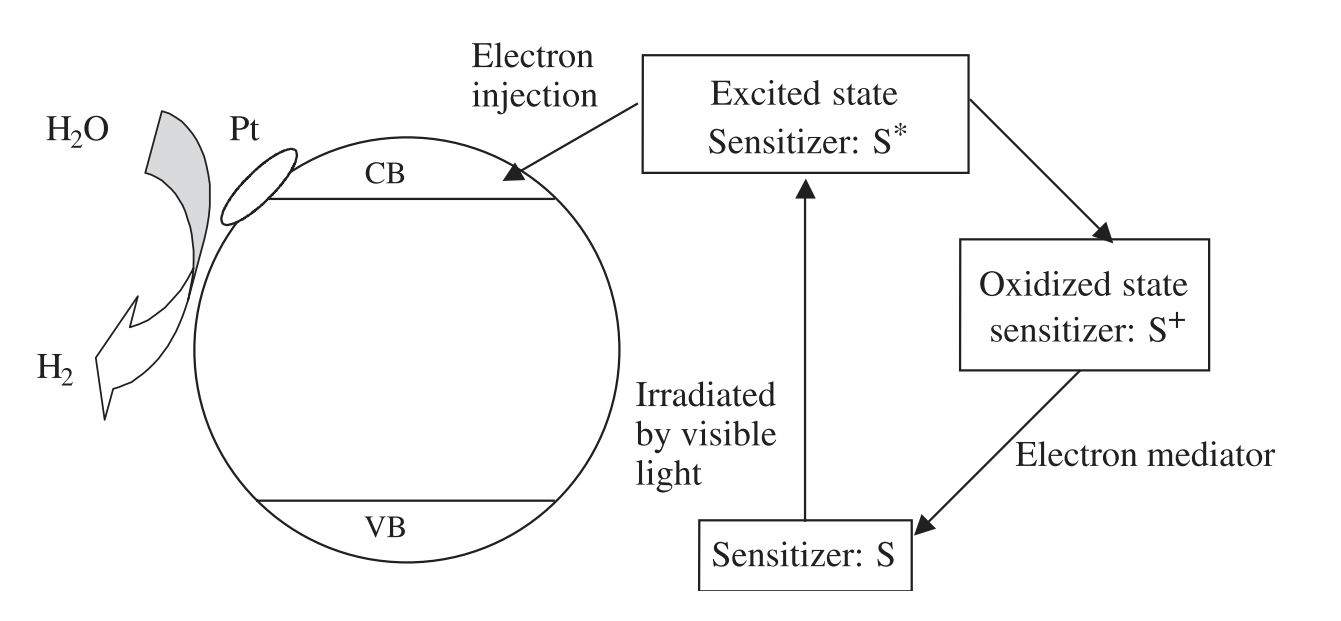
光生电子和空穴可以分别还原和氧化半导体吸附的反应,所以光催化制氢的基本机制是氧化还原反应。在光催化制氢反应中,半导体的导带电势应该比氢的还原电势更负(EH2/H2O),价带电势应该比氧的氧化电势更正(EO2/H2O),光解水制氢反应才能发生。TiO2光催化制氢机理所示:
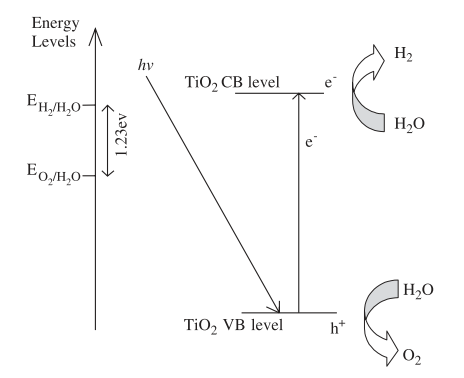
图1.1 TiO2光催化分解水制氢机理
TiO2虽然催化活性高、光生电子-空穴寿命长,但光解水制氢的能量转化效率仍然很低,主要有三个原因[6]:(1)光生电子-空穴对极易复合:光生电子与空穴快速复合并以非热能和光能的形式释放能量。(2)逆反应快速进行:水分解成氢和氧是一个能量增加的过程,因而逆反应很容易进行。(3)不能利用可见光:TiO2的带隙宽度约为3.2 eV只能利用紫外光,由于紫外光仅占太阳辐射能量的4%左右,可见光占50%左右,因此利用可见光的能力限制了光催化制氢的效率。
1.3提高TiO2光催化制氢的方法
因此,扩展光吸收范围、降低光生电子-空穴的复合成为制备高效TiO2光催化剂的重要因素。目前研究的主要方法有元素掺杂[7],半导体复合[8],染料敏化[9]和贵金属沉积等[10]。
1.3.1 元素掺杂
元素掺杂按照掺杂元素种类分为金属元素掺杂和非金属元素掺杂。金属离子掺杂在TiO2的晶格中,不仅可以扩展TiO2光吸收范围,增强太阳能的利用率,还可以抑制光生电子-空穴复合[11]。吴志伟[12]采用离子吸附和碳球模板法制备了Na、Mg和分别掺杂的TiO2超薄纳米空心球,拓宽了TiO2的带隙宽度,提高了材料的氧化还原电位。Dholam[13]等人采用射频磁控溅射法和溶胶-凝胶法制备了掺杂Cr和Fe的TiO2薄膜,研究了可见光下光催化制氢的方法。结果表明,Fe掺杂TiO2(15.5 μmol/h)的H2生成速率高于Cr掺杂TiO2(5.3 μmol/h),这是因为Fe离子能够同时捕获电子和空穴,从而避免复合,而Cr只能捕获一种电荷载流子。非金属掺杂元素目前采用的最多的是N元素,C、B、S和卤族元素也十分常见,与金属掺杂不同的是,非金属元素掺杂使扩展TiO2可见光催化活性,又不影响到其在紫外光范围内的催化活性[14]。Fuyun Pei[15]等人采用溶剂热法制备N掺杂TiO2复合N掺杂石墨烯,结果表明,NTNG在紫外光照射下的光催化效率比商用P25提高了13.1倍。Jian Yuan[16]等人采用尿素作为氮源制备了高比表面积的N掺杂TiO2样品,N掺杂后使得TiO2由锐钛矿相转变为金红石相,制氢效率明显提高。
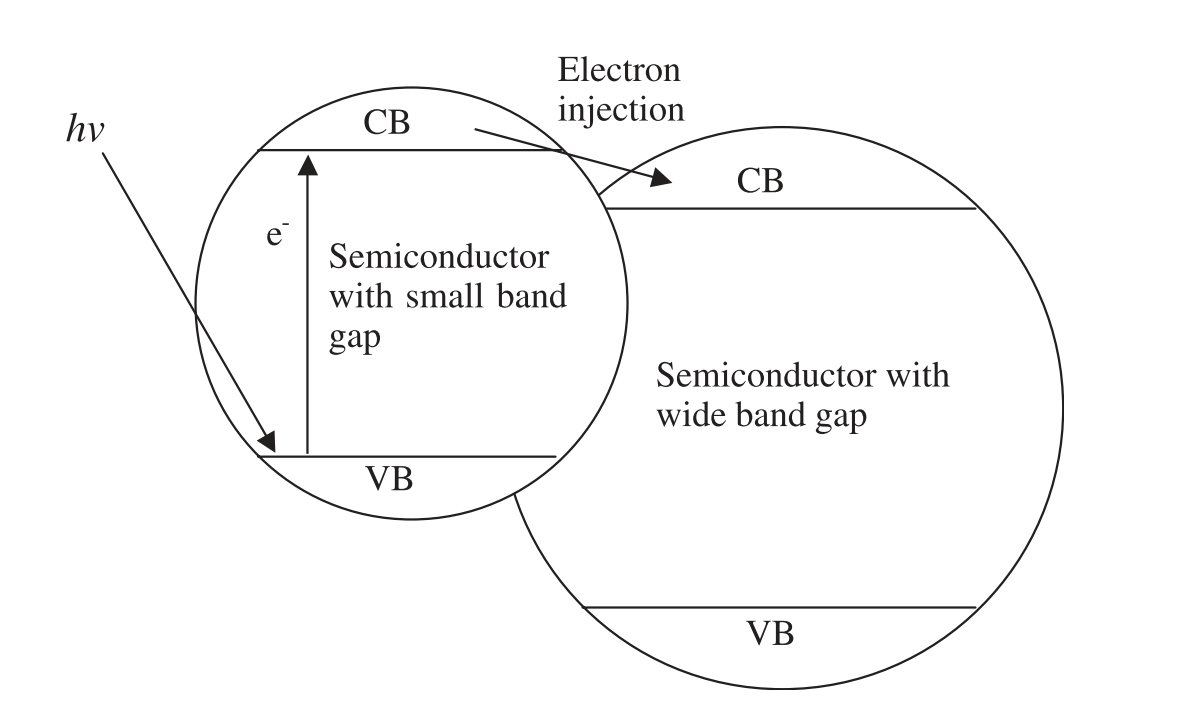
1.3.2 半导体复合
半导体复合可以提高电荷分离效果,扩宽光谱吸收范围,目前一般采用宽带隙较窄的半导体,比如,CdS,WO3,Al2O3、SnO2等[17]。Zichao Lian[18]等人通过离子交换方制备富勒烯(C60)增强介孔CdS/TiO2结构,C60团簇被引入到介孔CdS/TiO2的孔壁中,增强了催化剂的光稳定性和光催化活性。Jum Suk Jang[19]采用沉淀法和溶胶-凝胶法制备了CdS/TiO2纳米块状复合光催化剂,该复合光催化剂在可见光照射(λ≥420 nm)下,以含硫化物和亚硫酸盐为牺牲剂,产氢效率有明显提升。并研究了CdS/TiO2复合光催化剂的物理化学性质,优化了以含Na2S和Na2SO3为牺牲剂的可见光催化制氢的制备条件。齐中[7]等人采用水热法制备了TiO2/MoS2复合光催化剂,并研究了MoS2最优负载量,复合催化剂负载的不同贵金属(Pt、Pd、Ru)及其最优负载量,不同牺牲剂对光催化反应制氢活性的影响,和光催化剂的稳定性。研究结果表明,复合TiO2/MoS2能显著提高TiO2光催化制氢性能, 当MoS2的负载量为5 wt%,制氢速率最高为776.99μmol h-1 g-1是纯TiO2的4.92倍,商业P25的3.57倍。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: