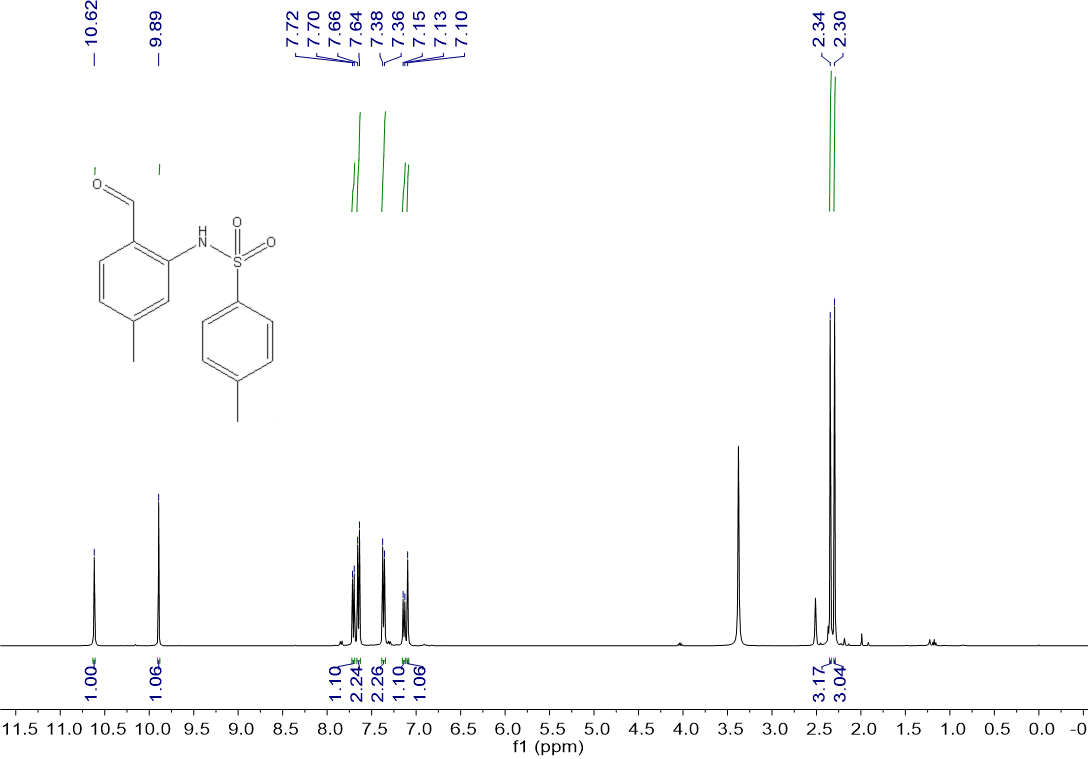
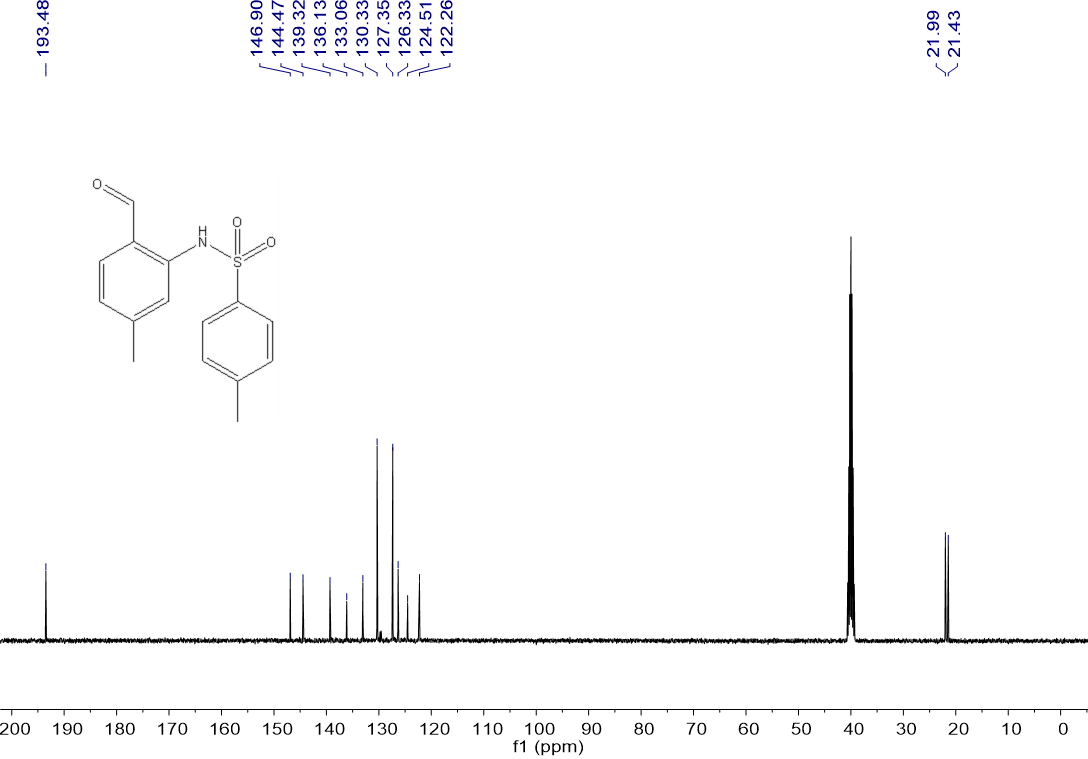
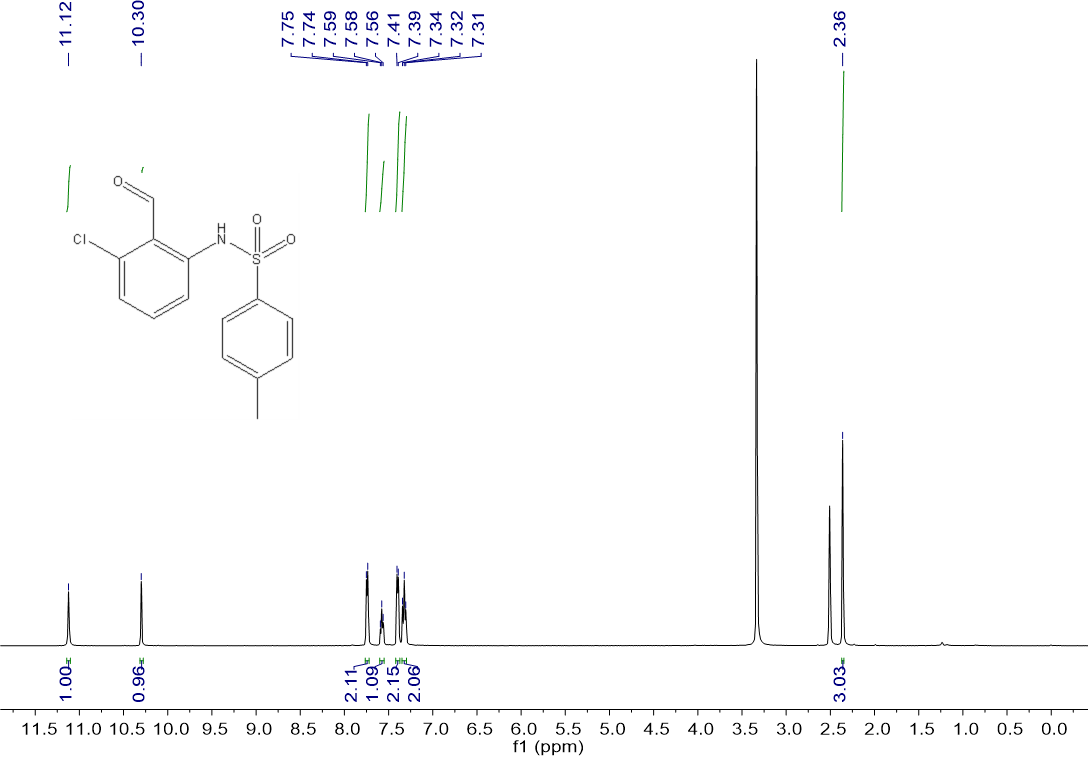
临时导向基团导向的C(sp2)-H活化合成苯磺酰胺衍生物毕业论文
2020-04-06 13:07:42
摘 要
苯磺酰胺衍生物可用来治疗艾滋病、阿尔茨海默症和丙型肝炎等多种疾病,还可用作杀菌、除草剂,是一种在医药和农药等领域用途非常广泛的化合物。由于其很好的应用性,苯磺酰胺衍生物的合成方法被广泛探索。过渡金属催化的临时导向基团策略是一种新型的合成方法,由于醛基的弱配位性及对氧化的敏感性等,醛基作为导向基团导向的C(sp2)-H键活化合成苯磺酰胺衍生物的方法还鲜有报道。本实验拟应用临时导向基团方法合成一系列苯磺酰胺衍生物。
本文采用间甲基苯甲醛作为底物,对甲基苯磺酰叠氮作为氮源探究该反应的最优条件。之后,在最优反应条件的基础上,我们进行了底物拓展并合成了一系列苯磺酰胺衍生物。实验发现,反应条件具有优良的底物多样性和值得更进一步探究的应用潜力。最后,本文绘制了反应可能的机理图并对反应机理进行了详细的解释,为相关的机理阐释提供了一种可靠思路。
关键词:磺酰叠氮;临时导向基团;苯甲醛;苯磺酰胺衍生物
Abstract
Benzene sulfonamide derivatives can be used for the treatment of various diseases such as AIDS, Alzheimer's disease and Hepatitis C. They can also be used as bactericidal and herbicides, which are compounds that widely used in Pharmaceuticals and Pesticides. Due to its good applicability, the synthesis of benzenesulfonamide derivatives has been extensively explored. The transition metal catalyzed transient directing group strategy is a novel synthesis method. Because of the weak coordination of aldehyde groups, method that aldehyde group as the directing group directed C(sp2)-H bond activation to synthesize benzenesulfonamide derivatives has rarely been reported. In this experiment, a series of benzenesulfonamide derivatives were synthesized using a transient directing group.
The optimal conditions for this reaction were investigated using meta-methylbenzaldehyde as a substrate, para-toluenesulfonyl azide as a nitrogen source. Afterwards, based on the optimal reaction conditions, we carried out the substrates development and synthesized a series of benzenesulfonamide derivatives. The experiment found that the reaction conditions have excellent substrate diversity and application potential worth further exploration. Finally, this paper drawed the possible mechanism diagram of the reaction and explained the reaction mechanism in detail, providing a reliable idea for the relevant mechanism interpretation.
Key words:Sulfonyl azide; Transient directing group; Benzaldehyde; Benzenesulfonamide derivatives
目录
摘 要 I
Abstract II
第1章 绪论 1
1.1引言 1
1.2 磺胺类药物介绍 1
1.3临时导向基团导向的C-H键活化反应研究现状 4
1.3.1临时导向基团导向的C-H键胺化反应 4
1.3.2醛基导向的C-H键活化反应 6
1.4 研究目的与意义 8
第2章 反应条件的优化 10
2.1引言 10
2.2 实验试剂、仪器设备及分析表征方法 10
2.2.1实验试剂 10
2.2.2 仪器设备 11
2.2.3 分析表征方法 11
2.3 反应条件优化 12
2.3.1 配体胺的优化 12
2.3.2 配体胺添加量的优化 13
2.3.3 添加剂的优化 14
2.3.4 三氟乙酸银添加量的优化 15
2.3.5 有机酸的优化 16
2.4 小结 16
第3章 底物适用性探究 18
3.1 引言 18
3.2 实验试剂、仪器设备及分析表征方法 18
3.2.1 实验试剂 18
3.2.2 仪器设备 19
3.2.3 分析表征方法 19
3.3 底物适用性探究 20
3.3.1 苯甲醛范围拓展 20
3.3.2 磺酰叠氮范围拓展 22
3.4 小结 25
第4章 机理探讨与产物表征数据 26
4.1 引言 26
4.2 机理探讨 26
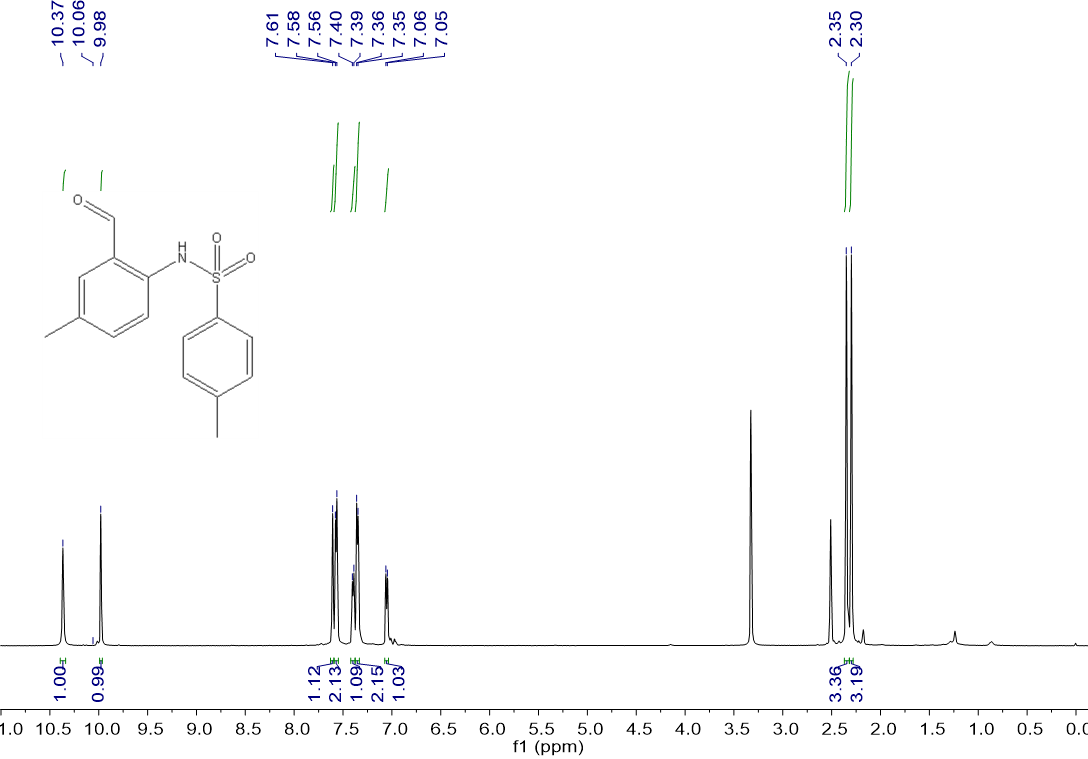
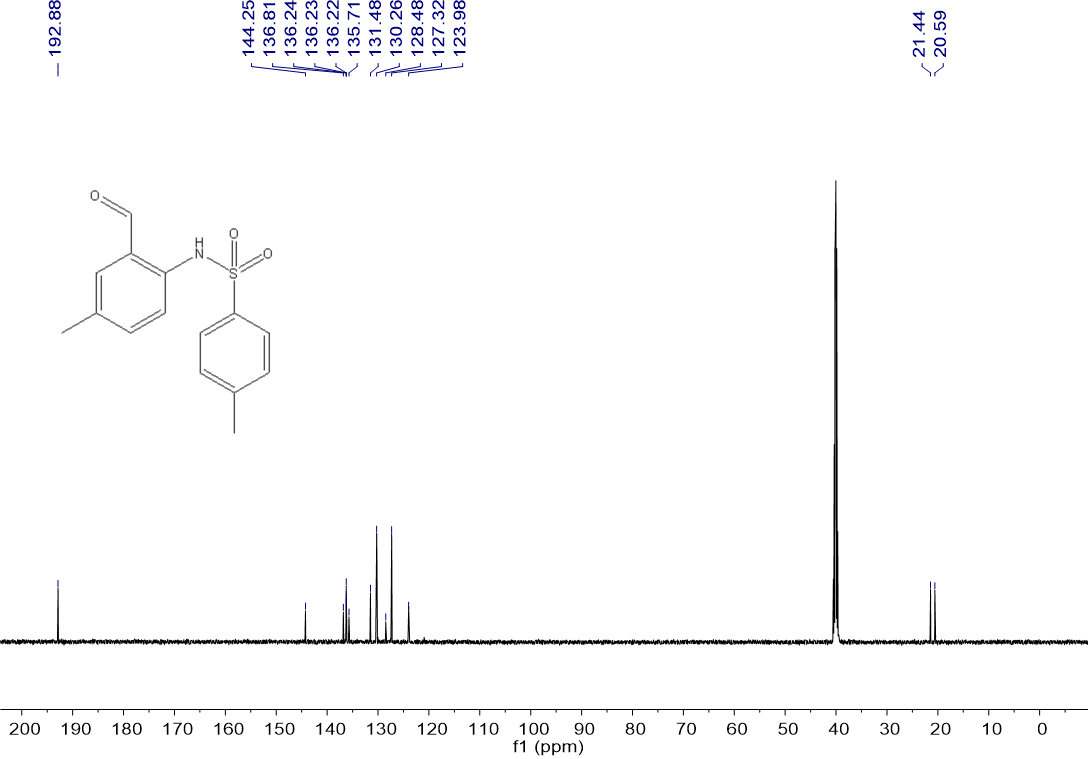
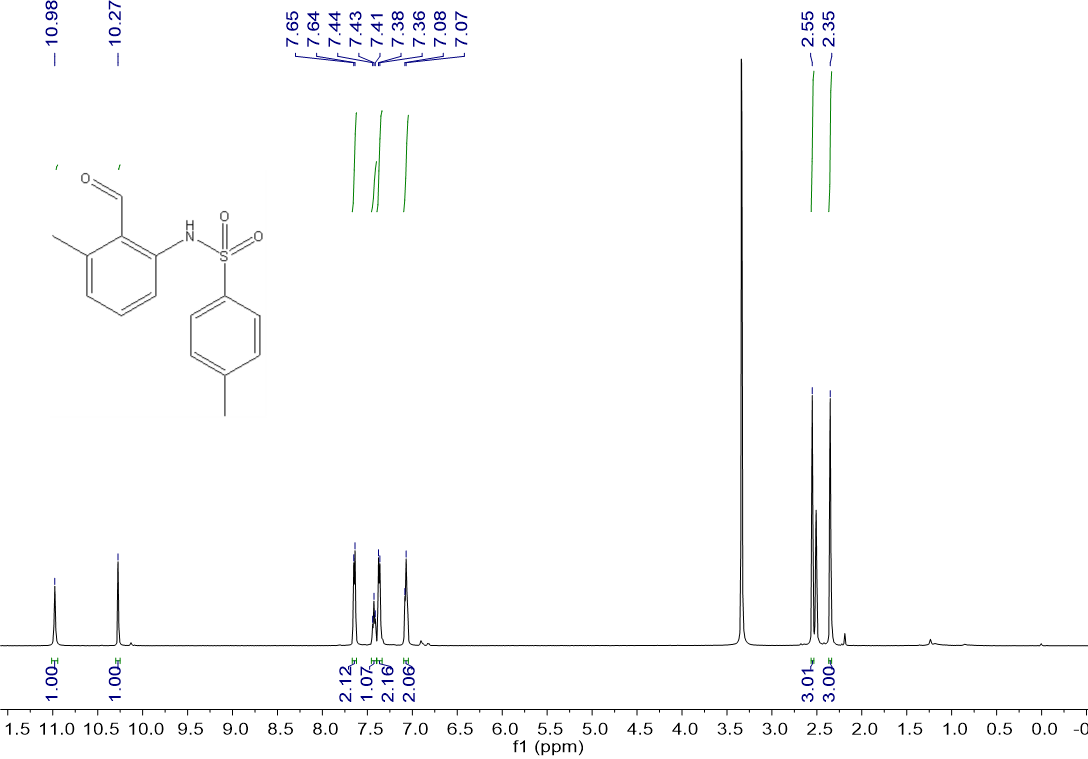
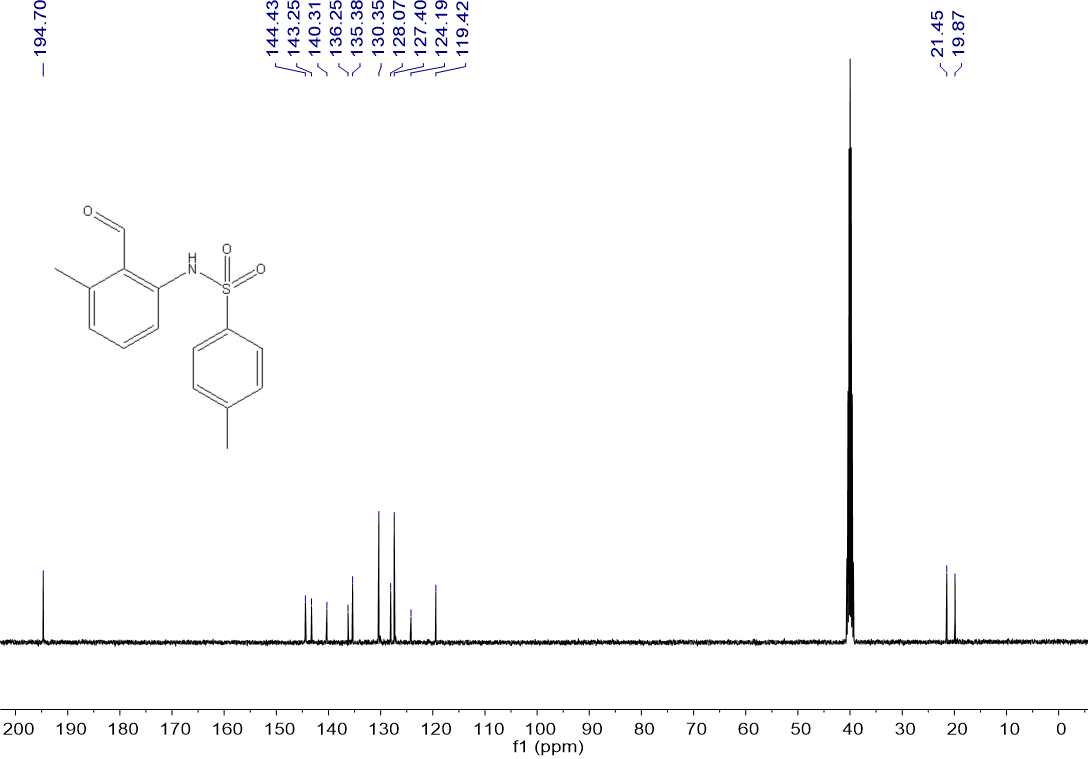
4.3 产物表征数据 27
4.4 本章小结 31
第5章 结论 32
参考文献 34
致 谢 36
附录 核磁谱图 37
第1章 绪论
1.1引言
苯磺酰胺衍生物是一种在医药和农药等领域用途非常广泛的化合物,具有不同的药用性能,可被用作RabGGTase抑制剂、MMP / TACE抑制剂及蛋白多糖抑制剂等。因此,其合成方法被广泛探索。过渡金属催化C-H键活化直接合成C-N键、C-C键等实现化合物功能化的方法是一种新兴的合成策略,将其应用于磺胺类药物的合成可以探究出非常简洁的合成路线。自Chang[1]等人开创了铑催化的磺酰叠氮与芳烃分子间的C-H键活化反应,利用磺酰叠氮实现C-H键酰胺化的反应被广泛报导。
由于醛基的弱配位能力,其作为导向基团在过渡金属催化下活化邻位C-H键的反应鲜有报道,直到临时导向基团概念的提出。2016年,张方林[2]等人的报道中提出了通过在醛基原位可逆形成亚胺作为临时导向基团的临时导向基团策略。醛基通过在原位形成亚胺作为临时导向基团可以超越能够导向C-H键活化的其他配位官能团,从而显著扩大苯甲醛的过渡金属催化C-H键官能化的范围。这种方法也可以应用于药物类似物的最新多样化等。
1.2 磺胺类药物介绍
作为水解酶的一种,GTP酶超家族可以和三磷酸尿苷(GTP)结合并将其水解。GTP酶超家族可被分为Ras、Rho/Rac、Rab、Arf和Ran等蛋白酶家族[3]。但Ras GTP酶超家族的成员经常在癌症中发生突变。因此,已经开发了通过抑制它们的异戊烯化酶FTase,GGTase I和RabGGTase来解决这些GTP酶的活性的抑制剂。与FTase和GGTase I相反,只有少数RabGGTase抑制剂已经开发出来。E. Anouk Stigter[4]等人报道了一种扩展的选择性抑制剂,该选择性RabGGTase抑制剂旨在建立抗癌治疗剂的新型药物开发程序。其结构如图:
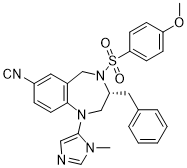
图1.1 选择性RabGGTase抑制剂结构式
TNF-α(肿瘤坏死因子-α)可参与炎症反应并介入众多疾病的病理过程,如类风湿性关节炎(RA)、局限性回肠炎、多发性硬化症、阿尔茨海默病及中风等。而促使TNF-α产生的关键酶——TNF-α转换酶(TACE)是上述疾病治疗的一个重要 “靶标”。因此,很多高效TACE抑制剂被开发出来,其对于包括RA在内的多种疾病具有很好疗效。研究发现基质金属蛋白酶(MMP)会在RA患者的滑膜组织中过度表达, MMP是一种与关节炎、肿瘤转移等相关的家族酶。而双重MMP / TACE抑制剂可能会具有较单一TACE抑制剂更好的疗效。Jeremy I. Levin[5]等人开发了一种高效合成外消旋苯二氮卓-磺酰胺异羟肟酸的方法。该酸类似物具有双重MMP / TACE抑制效果。其结构式如下:
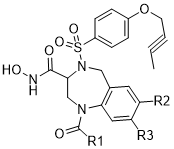
图1.2 双重MMP / TACE抑制剂结构式
司美匹韦[6] ( Simeprevir,SMV) 是一种可以用来治疗慢性丙型肝炎成年患者的代偿性肝病的口服药,作为一种新型的NS3/4A蛋白酶抑制剂,它可以阻断NS3/4A蛋白酶,而NS3/4A蛋白酶可以激活丙型肝炎病毒(Hepatitis C virus,HCV)的复制,因此,SMV可以用来抑制HCV在肝脏细胞中的复制从而治疗丙型肝炎。SMV由Medivir和强生联合开发。在美国,经食品和药物管理局批准,SMV可以与聚乙二醇干扰素和利巴韦林联合治疗丙型肝炎。在日本,SMV已经被批准用于治疗慢性丙型肝炎感染。其结构式如下:
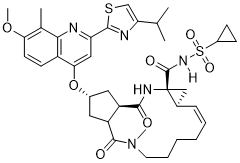
图1.3 司美匹韦结构式
蛋白多糖(chondroitin sulfate proteoglycans,CSPGs)由核心蛋白和共价连接的一个或多个线性糖氨多糖链 (glycosaminoglycan , GAG )构成,它存在于中枢神经系统(CNS)细胞外的基质中,对CNS的发育、成熟过程中正常功能的维持起着不可或缺作用,例如,在神经细胞的发育中影响其迁移和轴突生长,在神经细胞成熟后介入调节神经可塑性等[7]。因为蛋白多糖在关节损伤、疾病和衰老过程中的重要作用,所以针对防止聚蛋白多糖的降解正在被研究,而蛋白多糖抑制剂是能够有效的阻碍蛋白多糖的降解的一个重要抑制剂,其结构式如图:
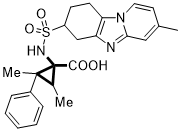
图1.4 蛋白多糖抑制剂结构式
作为对当今人类危害极大的心血管病的致病因子之一,血栓栓塞是医学研究的热门问题。研究表明,血栓烷A2 ( Thromboxane A2 ,TXA2 ) 可以诱导血小板聚集从而使血小板沉积,而血小板沉积是导致血栓栓塞的重要因素之一[8]。因此,开发出抑制血栓烷A2功能的血栓烷A2拮抗剂对人类健康具有重要意义。此外,白三烯D4也可以介导血栓病。关于单独的血栓烷A2拮抗剂或白三烯D4拮抗剂的药物开发被较多报道。安田信吾[9]等人开发了一种具有血栓烷A2和白三烯D4双重拮抗作用的磺胺类药物,可能会较单一拮抗剂有更好抗血栓效果。其结构式如下:
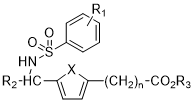
图1.5 双重血栓烷A2、白三烯D4抑制剂
1.3临时导向基团导向的C-H键活化反应研究现状
1.3.1临时导向基团导向的C-H键胺化反应
2011年,Frank Glorius[10]团队实现了Rh(III)催化室温下进行的N-新戊酰氧基苯甲酰胺与N-氯胺的直接C-H键胺化。该课题组先使用苯并异羟肟酸衍生物作为底物,N-取代的吗啉作为氮源,[RhCp*Cl2]2 (Cp*= 1,2,3,4,5-pentamethylcyclopentadienyl,1,2,3,4,5-五甲基环戊二烯)作为催化剂,CsOAc(醋酸铯)作为添加剂在室温下反应并得到合理收率。之后,在该反应条件的基础上进一步优化,探究N-新戊酰氧基苯甲酰胺(N-pivaloyloxybenzamide)作为底物的最佳反应条件。实验发现,在CsOAc中加入特戊酸(PivOH)能有效提高反应收率。其反应方程式如下图所示:
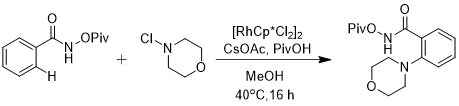
图1.6 铑(III)催化的N-新戊酰氧基苯甲酰胺的胺化反应
2013年,在Chang[1]等人的基础上,M. Ramu Yadav [11]的团队报道了Ru(II)催化的N-苯甲酰化磺酰亚胺(N-[m-methylbenzoyl]-MPS)与磺酰叠氮化合物的分子间芳烃邻位C-H键酰胺化。该反应的优化条件为[RuCl2(p-cymene)]2 (二氯双(4-甲基异丙基苯基)钌)(10 mol%)、六氟锑酸银(AgSbF6) (40 mol%) 以及KOAc (50 mol%)在120℃下的1,2-二氯乙烷(DCE)溶剂中反应24 h。之后在对该反应的适用性进行探究的过程中发现,具有不同取代基团的苯的底物以及磺酰叠氮均能得到中等及以上的收率。该酰胺化反应兼具化学选择性和位点选择性。
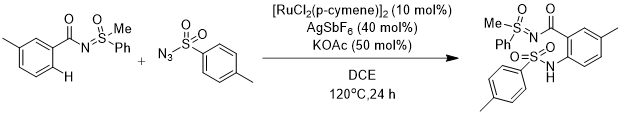
图1.7 铑(II)催化的N-苯甲酰化磺酰亚胺的酰胺化反应
同年,M. Bhanuchandra[12]等人报道了过渡金属催化的芳香酮邻位C-H键酰胺化反应。该反应采用便宜、易于制备和空气稳定的Ru(II)作为催化剂,以苯乙酮作为反应底物,以对甲基苯磺酰叠氮作为氮源探究实验的最佳反应条件,得出了以[RuCl2(p-cymene)]2作催化剂,AgSbF6作添加剂,Cu(OAc)2H2O 作为碱,1,2-二氯乙烷作溶剂在100℃下反应24 h的最佳反应条件。在没有碱存在的条件下该反应不能进行。对于具有不同取代基的苯甲醛底物和苯磺酰叠氮,反应均具有较好的适用性。
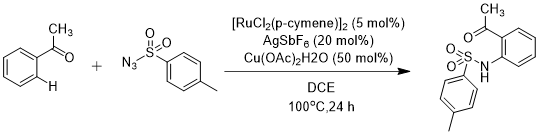
图1.8 铑(II)催化的苯乙酮邻位C-H键酰胺化反应
2014年,Jinwoo Kim[13]等人开发了温和条件下铱催化弱配位羰基导向的C(sp2)-H键酰胺化。在Dixneuf[14]等人的启发下,该课题组在反应中加入适当的酸添加剂抑制碱性配体的结合亲和力,从而增加弱结合底物如酯和酮对催化剂金属中心的配位效率。以苯甲酸乙酯为底物,反应在25℃时的最佳反应条件为: [IrCp*Cl2]2作为催化剂,AgNTf2 、AcOH/Li2CO3 作添加剂,DCE作溶剂,反应时间为12 h,收率为75%,在50℃时,收率可达98%。该反应条件对于芳香酮类及烯酮类均适用,且在常温下具有较好的底物适用性。
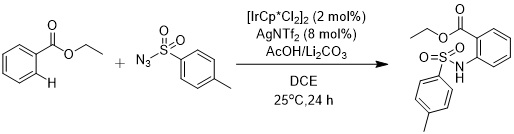
图1.9 铱催化的苯甲酸乙酯邻位C-H键酰胺化反应
2015年,崔秀灵[15]课题组报道了温和高效的铱催化、弱配位羧基导向的邻位C-H键酰胺化反应。该反应提供了一种邻氨基苯甲酸的新型合成方法。课题组首先以邻氟苯甲酸为底物,以对甲基苯磺酰叠氮为氮源探究最佳反应条件:催化剂[IrCp*Cl2]2(2 mol%),配体AgNTf2(8 mol%),HOAc(15 mol%),Li2CO3(15 mol%)、 溶剂DCE,反应温度80℃,反应时间12 h。在此最佳反应条件的基础上,该报道还探究了不同对位取代苯甲酸底物的双酰胺化,探究表明,双酰胺化也能得到较好收率。
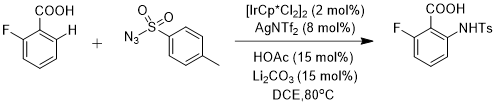
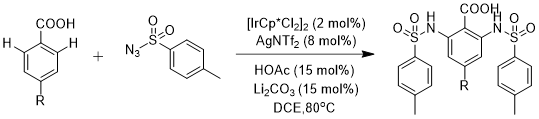
图1.10 铱催化的苯甲酸邻位C-H键酰胺化反应
2017年,Han S H[16]等人报道了Ir(III)催化的苯甲酸与磺酰叠氮直接酰胺化得到邻氨基苯甲酸的反应。该反应以2-甲氧基苯甲酸和4-甲氧基苯磺酸叠氮为反应物探究反应最佳条件。该反应条件与崔秀灵课题组提出的方案类似,不同之处在于该方案采用NaOAc做为添加剂。此外,该报道对全部底物拓展产物进行了详细的生物活性测试。
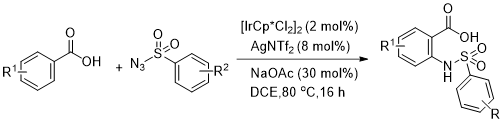
图1.11 铱催化的苯甲酸邻位C-H键酰胺化反应
1.3.2醛基导向的C-H键活化反应
2011年,Emmanuelle Dubost[17]课题组报道了醛基的邻位C(sp2)-H键溴化反应。该过程通过三步反应由苯甲醛合成邻溴苯甲醛。其中钯催化的选择性邻位溴化是关键步骤。由于醛基的弱配位性等,该反应将醛基转化为甲氧基肟,以甲氧基肟作为导向基团实现甲氧基肟邻位溴化。之后,酸解甲氧基苯甲酰肟得到邻溴苯甲醛。
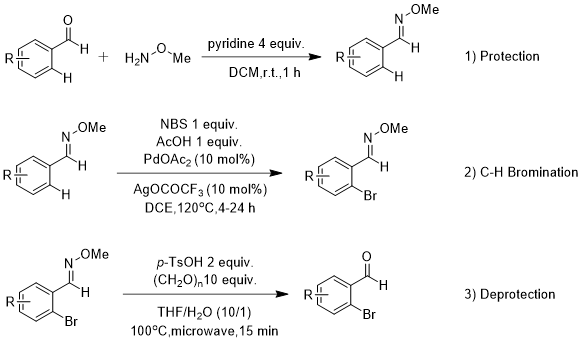
图1.12 三步实现醛基邻位溴化反应
2016年,张方林[2]等人报道了醛基导向的C(sp3)-H键芳基化,并且创造性的提出了醛基作为导向基团导向邻位C(sp3)-H键芳基化的亚胺临时导向基团机理。该反应采用2-氨基苯甲醛和4-碘苯甲醚作为反应物探究反应最佳条件。根据醛基能与氨基酸形成亚胺中间体的特性,采用甘氨酸作为临时导向基团并采用醋酸作溶剂使反应提高到52%,考虑到反应过程中形成的亚胺有分解,使AcOH:H2O为9:1稀释亚胺中间体使反应达到71%的核磁产率,最后通过改变碘苯的量以消除二芳基化产物使反应产率达到81%。该反应具有良好的底物适用性并且将该反应条件应用于脂肪酮也具有良好的产物收率。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: